Abundância isotópica
Referência : Ribeiro, D., (2014) Abundância isotópica, Rev. Ciência Elem., V2(3):219
Autores: Daniel Ribeiro
Editor: Jorge Gonçalves
DOI: [http://doi.org/10.24927/rce2014.219]

A abundância isotópica numa amostra é a fracção do número de átomos de um dado isótopo de um elemento em relação ao número total de átomos desse elemento presentes na amostra.[1]
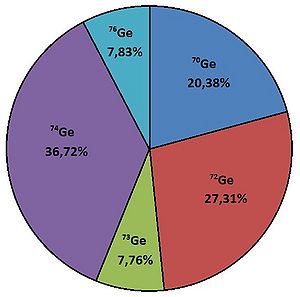
Salvo algumas exceções, os elementos possuem diversos isótopos que surgem na Natureza em diferentes percentagens (ver figura 1). Abundância isotópica natural é a abundância isotópica encontrada na Natureza.[1]
A composição isotópica de um elemento deve indicar a abundância relativa de cada um dos seus isótopos.[2] A abundância de um isótopo é um valor necessário para os cálculos de massas atómicas (relativas ou não) de elementos químicos porque a massa atómica é a média pesada das massas isotópicas correspondentes.
Assim, o cálculo de uma massa atómica relativa pode ser dado, matematicamente, por
\(A_r = w(1)\times A_r(1)+w(2)\times A_r(2)+w(3)\times A_r(3)+\cdots\)
em que \(w(i)\) é a abundância relativa do isótopo \(i\) de massa atómica \(A_r(i)\).[3] Por exemplo, para o germânio, \({}_{32}\mbox{Ge}\), virá:
\(A_r(\mbox{Ge}) = 0,2038\times 69,9242474+0,2731\times 71,9220758+0,0776\times 72,9234589+0,3672\times 73,9211778+0,0783\times 75,9214026\)
\(\Leftrightarrow A_r(\mbox{Ge}) = 72,64\)
A tabela periódica abaixo pode ser utilizada para consultar os valores das abundâncias isotópicas de diversos isótopos, bem como as massas isotópicas relativas e as massas atómicas relativas de cada elemento químico. Poderá também consultar um arquivo com os dados referidos para todos os elementos químicos aqui.
| 1 | 18 | ||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
1
|
2 | 13 | 14 | 15 | 16 | 17 | |||||||||||||
2
|
|||||||||||||||||||
3
|
3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | |||||||||
4
|
|||||||||||||||||||
5
|
|||||||||||||||||||
6
|
* | ||||||||||||||||||
7
|
** | ||||||||||||||||||
| * | |||||||||||||||||||
| ** |
Referências
- International Union of Pure and Applied Chemistry (IUPAC): Glossary of terms used in nuclear analytical chemistry, consultado em 14/05/2012.
- International Union of Pure and Applied Chemistry (IUPAC): Isotopic compositions of the elements 2009 (IUPAC Technical Report), consultado em 14/05/2012.
- C. Corrêa, F. P. Basto, N. Almeida, Química, 1ª edição, Porto: Porto Editora, 2008, ISBN: 978-972-0-42248-4.
Criada em 14 de Maio de 2012
Revista em 15 de Maio de 2012
Aceite pelo editor em 18 de Maio de 2012