Raio iónico
Referência : Fernandes, R.F., (2014) Raio iónico, Rev. Ciência Elem., V2(1):130
Autores: Ricardo Ferreira Fernandes
Editor: Jorge Gonçalves
DOI: [http://doi.org/10.24927/rce2014.130]

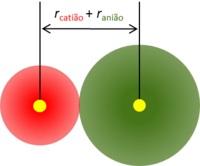
O raio iónico corresponde à medida do raio de um ião num composto cristalino iónico, considerando-se que os iões apresentam forma esférica. A distância entre o núcleo do catião e do núcleo do anião equivale à soma dos dois raios iónicos (figura 1).
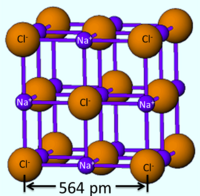
O conceito de raio iónico foi desenvolvido independentemente, em 1920, pelo químico norte-americano Linus Pauling (1901-1994) e pelo químico suíço Victor Goldschmidt (1888-1947), para coligir dados cristalográficos gerados pela técnica de difracção de raios-X. Esta técnica fornece o comprimento da unidade de célula de um cristal, porém não distingue a fronteira entre os iões que a compõem. Por exemplo, a célula unitária do cloreto de sódio (NaCl) tem um comprimento de 564 pm (figura 2) o que corresponde ao dobro do raio iónico de cada um dos iões:
Por comparação de estruturas cristalográficas de vários compostos iónicos, Linus Pauling, atribuiu o valor de 140 pm ao ião O2-. Deste modo, conhecendo-se o raio de um dos iões, e, sabendo que a soma dos raios iónicos está relacionada com o comprimento da unidade de célula do cristal, pode calcular-se o valor do raio dos outros iões.

Em geral o raio iónico diminui com o aumento da carga positiva e aumenta com o aumento da carga negativa. Os catiões são sempre mais pequenos que o átomo, devido à diminuição da repulsão electrão-electrão. Os aniões são sempre maiores que o átomo, devido à introdução de mais um electrão na camada de valência, o que provoca um aumento na repulsão electrão-electrão, traduzindo-se numa expansão da nuvem electrónica. Para iões com carga igual, apresenta maior raio iónico aquele que tiver o maior número atómico. O raio iónico, de uma forma semelhante ao raio atómico, é uma propriedade periódica, que aumenta monotonamente ao longo de um grupo e diminui genericamente ao longo de um período. A figura 3 apresenta a variação do raio atómico e do raio iónico para alguns elementos da tabela periódica.
Criada em 18 de Abril de 2011
Revista em 31 de Março de 2014
Aceite pelo editor em 31 de Março de 2014
![2 \times [r_{\text{cati} \tilde{a} \text{o} } (\text{Na}^+) + r_{\text{ani} \tilde{a} \text{o}} (\text{Cl}^-) ] = 564 \text{ pm}](/wiki/images/math/a/b/b/abb93ca7425fb93edd0cc25eec2c0e3e.png)