Reacção química
Referência : Fernandes, R.F., (2015) Reação química, Rev. Ciência Elem., V3(3):179
Autor: Ricardo Ferreira Fernandes
Editor: Jorge Gonçalves
DOI: [http://doi.org/10.24927/rce2015.179]
Uma reacção química é um processo em que determinadas substâncias (os reagentes) se combinam entre si para originar novas substâncias (os produtos de reacção). Uma reacção pode ser elementar (ocorre num só passo ou processo elementar) ou ocorrer em vários passos elementares em que se formam e transformam substâncias que se denominam intermediários.
A descoberta do oxigénio, em 1774, por Joseph Priestley e Karl Wilhem, foi muito importante para a compreensão das reacções químicas. Antoine Lavoisier, que seguia os trabalhos de Priestley, foi capaz de explicar o papel do oxigénio na combustão e na respiração, o que o levou a uma melhor compreensão da forma como as substâncias se combinavam e originavam novos compostos. Lavoisier observou que durante uma reacção num sistema fechado a massa total dos materiais presentes não se alterava no decorrer da reacção, princípio que é hoje conhecido como a lei da conservação da massa.
Outro princípio fundamental para a compreensão das reacções químicas, que está na base da estequiometria, é a lei das proporções definidas, observada por Joseph Proust, em 1806, que demonstrou que os elementos constituintes de qualquer composto estão presentes sempre na mesma proporção mássica.
Em 1808, Jonh Dalton, baseado nos dois princípios anteriores, e nas suas observações, expandiu a lei de Proust propondo a lei das proporções múltiplas, em que as massas de um elemento A que se combinam com uma dada massa de um elemento B estão sempre numa razão de números inteiros pequenos.
As observações de Lavoisier, Proust e Dalton permitiram a Dalton propor que a matéria era constituída por átomos (corpúsculos) que se combinam entre si para originar novos compostos. Assim, estes três princípios foram extremamente importantes na compreensão das reacções químicas, o que esteve na base do desenvolvimento da Química como uma ciência quantitativa.
As reacções químicas envolvem o rearranjo dos átomos, com quebra e formação de ligações, originando novos compostos. As reacções podem ser espontâneas, quando não necessitam da acção de nenhum factor externo para ocorrerem, ou não-espontâneas (ou provocadas) se necessitarem de um factor externo para ocorrerem, como por exemplo, o calor, a electricidade ou a luz.
As reacções químicas só ocorrem espontaneamente se forem termodinamicamente favoráveis, Por exemplo, algumas reacções não ocorrem à temperatura ambiente, porém, a partir de um determinado valor de temperatura, a reacção passa a ser termodinamicamente favorável e pode ocorrer numa extensão apreciável.
Para além dos factores termodinâmicos, a cinética da reacção é também importante. Por exemplo, a forma mais estável do carbono é a grafite, porém, a reacção de transformação do diamante em grafite, apesar de ser termodinamicamente favorável, não se observa porque é muitíssimo lenta.
Todas as reacções químicas podem ser descritas por equações, que representam através de símbolos, a composição do sistema no início (reagentes) e fim da reacção (produtos da reacção) ao nível atómico e molecular (formação e/ou quebra de ligações). De acordo com a natureza da transformação química, as reacções podem ser classificadas em diferentes tipos, nomeadamente:
HCl(aq) + H2O(l) 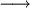 Cl-(aq) + H3O+(aq) Cl-(aq) + H3O+(aq) |
ácido-base |
CH4(g) + 2O2(g) 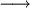 2H2O(l) + CO2(g) 2H2O(l) + CO2(g) |
combustão |
C12H22O11(s) 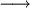 12C(s) + 11H2O(g) 12C(s) + 11H2O(g) |
decomposição |
Cl2(g) + KBr(aq) 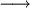 KCl(aq) + Br2(l) KCl(aq) + Br2(l) |
deslocamento |
Sn2+(aq) + 2Fe3+(aq) 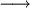 Sn4+(aq) + 2Fe2+(aq) Sn4+(aq) + 2Fe2+(aq) |
oxidação - redução |
AgNO3(aq) + NaCl(aq) 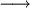 AgCl(s) + NaNO3(aq) AgCl(s) + NaNO3(aq) |
precipitação |
C(s) + O2(g) 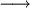 CO2(g) CO2(g) |
síntese |
No dia-a-dia, no nosso planeta, milhares de reacções químicas decorrem em simultâneo, começando pelas reacções no nosso organismo responsáveis pela vida, a combustão dos combustíveis fosseis que nos aquecem e fazem mover os transportes, as reacções nos eléctrodos das pilhas ou baterias que permitem o funcionamento dos telemóveis e equipamentos portáteis, até reacções prejudiciais como a formação de chuvas ácidas na atmosfera.
A manipulação e controlo das reacções químicas, desde a descoberta pré-histórica dos modos de obtenção do fogo, passando pela extracção e isolamento dos metais, até à produção de medicamentos, teve um papel fundamental no desenvolvimento da civilização humana e aumento da esperança de vida das populações. Assim, grande parte dos bens que possuímos não existiriam sem o recurso a reacções químicas, como por exemplo, as roupas que vestimos feitas à base de nylon ou poliéster, perfumes, detergentes, alimentos, produtos de cosmética, tintas, acumuladores de energia (baterias e pilhas), fertilizantes, e quase tudo que nos rodeia no mundo actual.
Referências
http://goldbook.iupac.org/C01033.html, consultado em 19/02/2010.
http://www.chemheritage.org/classroom/chemach/forerunners/priestley.html consultado em 19/02/2010.
http://www.chemheritage.org/classroom/chemach/forerunners/lavoisier.html consultado em 19/02/2010.
http://antoine.frostburg.edu/chem/senese/101/glossary/c.shtml consultado em 19/02/2010.
http://www.wiredchemist.com/chemistry/instructional/intro_chem_reactionsoverview.html consultado em 19/02/2010.
http://www.chemheritage.org/explore/matter-dalton.html consultado em 19/02/2010.
http://web.lemoyne.edu/~giunta/proust.html consultado em 19/02/2010.
http://web.lemoyne.edu/~giunta/proust2.html consultado em 19/02/2010.
http://web.lemoyne.edu/~giunta/dalton.html consultado em 19/02/2010.
http://www.fordhamprep.org/gcurran/sho/sho/lessons/lesson82.htm consultado em 19/02/2010.
Criada em 7 de Março de 2010
Revista em 12 de Agosto de 2010
Aceite pelo editor em 13 de Setembro de 2010

