Diamante
Referência : Ribeiro, D., (2014) Diamante, Rev. Ciência Elem., V2(2):175
Autores: Daniel Ribeiro
Editor: Jorge Gonçalves
DOI: [http://doi.org/10.24927/rce2014.175]

O diamante é uma das formas alotrópicas do elemento químico carbono. O carbono pode ser encontrado na Natureza em três diferentes formas simples: amorfo, grafite e diamante.[1]
A grafite é a forma estável do carbono a 1 atm e 25 ºC, mas a velocidade do processo espontâneo: C (diamante) → C (grafite), a esta pressão e temperatura é extremamente lenta. São necessários milhões de anos para que o diamante se transforme em grafite.
O diamante natural formou-se no interior da Terra a partir de grafite sujeita a pressões enormes durante milhões de anos. A estrutura do diamante revela-se termodinamicamente estável a pressões superiores a 6 GPa, à temperatura ambiente. No entanto, quando submetido a pressões idênticas à pressão atmosférica, o diamante passa a encontrar-se num estado metastável – um estado de equilíbrio estável diferente do equilíbrio termodinâmico. A baixas pressões o diamante converte-se rapidamente em grafite, para temperaturas acima de 1900 K, em atmosferas inertes.[2]
De todas as pedras preciosas, os diamantes são as de valor mais elevado. Historicamente, o diamante era um símbolo de força, coragem e invencibilidade.[3] Os registos existentes de exploração de diamantes datam de há mais de 4000 anos. Nessa altura, e desde então, esses cristais têm sido utilizados como decorações de peças religiosas ou como talismãs. Acredita-se que foi Alexandre, o Grande, que, no século IV a.C., trouxe os primeiros diamantes para a Europa.[3] Até ao século XVIII, a Índia era, quase exclusivamente, o único país onde a extração deste material era feita. Posteriormente, também se encontraram reservas de diamantes, primeiro no Brasil e depois na África do Sul. A partir do século XX, a África do Sul e outros países africanos assumiram-se como os principais exportadores mundiais de diamantes.
As propriedades físicas do diamante fazem deste um material extremamente atrativo. É o material mais duro conhecido até à data e, por isso, figura no máximo da escala de Mohs – escala que compara a dureza dos materiais; o diamante possui classificação 10 nessa escala. Além de duro, este material possui uma condutividade elétrica muito baixa. Este último facto deve-se à estrutura cristalina do diamante[4] – cúbica (ver figura 1) – e ao tipo de ligação química[4] existente entre os átomos de carbono no mesmo – covalente com hibridização sp3.
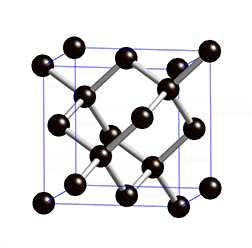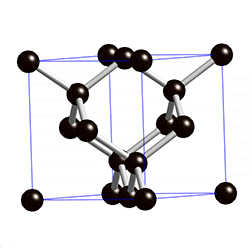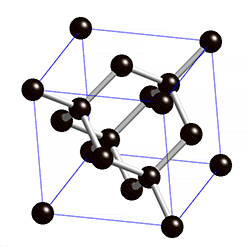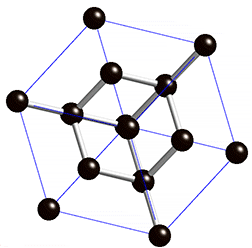
Além disto, o diamante possui uma condutividade térmica invulgarmente elevada para um material não metálico. É opticamente transparente para a radiação visível e algumas regiões do infravermelho e possui um elevado índice de refração.
Alguns diamantes são utilizados na indústria como ferramentas de corte. Nesse sentido, foram elaboradas técnicas de produção de diamantes sintéticos na década de 1950[4], submetendo a grafite a pressões e temperaturas muito elevadas. Nos últimos anos, a tecnologia de produção de diamantes sintéticos permitiu ao Homem produzir finas placas de diamante (de cerca de 1 mm de espessura) que possuem propriedades bastante próximas das do diamante de dimensões regulares.[4] Isto possibilitou o revestimento de lâminas, brocas e serras para melhorar a sua capacidade de corte ou perfuração.
Referências
- ↑ [1] D. R. Lide, ed., CRC Handbook of Chemistry and Physics, 89th edition, Boca Raton, Fla. London: CRC, 2008, ISBN: 978-1420066791.
- ↑ [2] IUPAC Gold Book: Diamond, consultado em 15/11/2011. (http://goldbook.iupac.org/PDF/D01671.pdf).
- ↑ [3] M. Dundek, Diamonds, 3rd edition, London: Noble Gems, 2009, ISBN: 978-0-9537884-3-9.
- ↑ [4] W. Callister, Materials Science and Engineering: An Introduction, Interactive MSE, 4th edition, New York: John Wiley & Sons, 1997, ISBN: 978-0-471-16867-6.
- ↑ [5] Wikimedia Commons: Diamond Cubic-F lattice animation, consultado em 15/11/2011 (http://upload.wikimedia.org/wikipedia/commons/2/22/Diamond_Cubic-F_lattice_animation.gif)
Criada em 5 de Dezembro de 2013
Revista em 9 de Dezembro de 2013
Aceite pelo editor em 12 de Dezembro de 2013

