Estequiometria
Referência : Lima, L.S., (2014) Estequiometria, Rev. Ciência Elem., V2(4):312
Autor: Luis Spencer Lima
Editor: Jorge Gonçalves
DOI: [http://doi.org/10.24927/rce2014.312]

A estequiometria é a parte da Química que se dedica ao estudo das proporções quantitativas entre reagentes e produtos numa reacção química. Baseia-se nos princípios da conservação da massa (Lei de Lavoisier), das proporções definidas (Lei de Proust) e das proporções múltiplas de Dalton. Através de cálculos matemáticos denominados cálculos estequiométricos, é possível determinar, por exemplo, a quantidade necessária e suficiente (quantidade estequiométrica) de um reagente para reagir com outro, o reagente limitante e o rendimento de uma reacção.
A raiz etimológica do termo “estequiometria” é grega, obtida por combinação das palavras stoikheïon (elemento) e métron (medida).
aA + bB 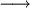 xX + yY
xX + yY
Na equação, a, b, x e y são designados por coeficientes estequiométricos. A estequiometria desta reacção refere-se ao facto que a moles de A reagem com b moles de B para se formarem x moles de X e y moles de Y. As proporções estequiométricas são sempre efectuadas numa base molar (e.g. é errado considerar que a gramas de A reagem com b gramas de B). A estequiometria de uma reacção pode ser bastante complexa ou até mesmo desconhecida. Por exemplo, a reacção de decomposição térmica do acetaldeído (CH3CHO) resulta na formação de metano (CH4) e monóxido de carbono (CO) como principais produtos da reacção, mas também se formam pequenas quantidades de outros produtos como acetona, etano ou diacetil. Por isso, a decomposição térmica do acetaldeído é um exemplo de um conjunto de reacções com uma estequiometria complexa.[1,2]
Para a reacção de combustão da glicose (C6H12O6) traduzida pela equação química seguinte
C6H12O6(s) + 6O2(g) 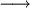 6CO2(g) + 6H2O(l)
6CO2(g) + 6H2O(l)
as proporções estequiométricas entre as substâncias intervenientes são as seguintes: uma mole de glicose para seis moles de dioxigénio, seis moles de dióxido de carbono para seis moles de água, uma mole de glicose para seis moles de dióxido de carbono, etc. Por isso, se se pretender fazer reagir na totalidade 10,0 g de glicose (= 0,0555 mol), deve utilizar-se, no mínimo, 0,333 mol de O2 (= 6 × 0,0555 mol), que corresponde à quantidade estequiométrica necessária. Caso a quantidade de glicose reaja na totalidade de acordo com a reacção indicada, formam-se 0,333 mol de H2O e de CO2. Estas proporções quantitativas entre as diferentes substâncias constituem a base da estequiometria.
Referências
1. http://goldbook.iupac.org/S06026.html, consultado em 21/12/2009.
2. K. S. Gupte, J. H. Kiefer, R. S. Tranter, S. J. Klippenstein, L. B. Harding, Proc. Comb. Inst. 31 (2007) 167-174.
Criada em 5 de Janeiro de 2010
Revista em 14 de Julho de 2010
Aceite pelo editor em 13 de Setembro de 2010

