Electrólise
Referência : Fernandes, R.F., (2015) Eletrólise, Rev. Ciência Elem., V3(1):019
Autor: Ricardo Ferreira Fernandes
Editor: Jorge Gonçalves
DOI: [http://doi.org/10.24927/rce2015.019]
Etimologicamente, electrólise significa "decomposição pela electricidade". A electrólise é, assim, um processo que utiliza corrente eléctrica para promover uma reacção química não espontânea. Para isso, um gerador de corrente eléctrica contínua é ligado aos eléctrodos de uma célula electrolítica forçando os electrões a participar em reacções provocadas de oxidação num dos eléctrodos (o ânodo) e de redução no outro eléctrodo (o cátodo).
No ano de 1800, os cientistas ingleses William Nicholson (1753-1815) e Anthony Carlisle (1768-1840), quando tentavam reproduzir as experiências de Allesandro Volta (1745-1827), com o objectivo de analisar as cargas eléctricas usando um electroscópio previamente desenvolvido por Nicholson, verificaram que ao inserirem os dois fios condutores metálicos provenientes da pilha de Volta num recipiente com água, se libertavam bolhas gasosas nas superfícies dos fios condutores (hidrogénio e oxigénio).[1] Posteriormente, em 1807, o químico inglês Sir Humphry Davy (1778-1840) fez passar uma corrente eléctrica através de hidróxido de potássio e hidróxido de sódio fundidos, isolando os elementos potássio e sódio, respectivamente. Davy prosseguiu os seus estudos com metais alcalino-terrosos, tendo isolado de forma semelhante o magnésio, o cálcio, o estrôncio e o bário. Em 1834, Michael Faraday (1791-1867) introduziu, por sugestão do polímato Rev. William Whewell (1794-1866), o termo electrólise que deriva do grego electro + lysis e significa decomposição por acção da electricidade.[2]
No quotidiano, a electrólise é um processo muito usado na preparação e purificação de metais, como por exemplo, na obtenção do alumínio a partir do mineral bauxite, ou na refinação do cobre na etapa final da extracção.
A electrólise é também utilizada para a obtenção industrial de algumas substâncias (compostas e elementares), como por exemplo, o clorato de potássio, o di-hidrogénio, o dicloro, o hidróxido de sódio e clorato de sódio.
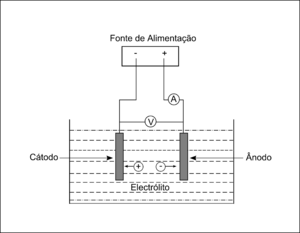
A electrólise também está presente nos processos de electrodeposição, nomeadamente no processo de galvanoplastia, no qual se pretende o revestimento de uma superfície condutora através da deposição, por acção de uma corrente eléctrica, de iões de um dado metal. A superfície que vai receber o revestimento metálico é ligada ao pólo negativo de uma fonte de alimentação comportando-se como um cátodo. O metal que vai fornecer o revestimento é ligado ao pólo positivo e comporta-se como ânodo. Quando a fonte de alimentação é ligada, a acção da corrente eléctrica que flui no circuito provoca a redução (no cátodo) do catião em solução e a oxidação do metal (no ânodo) (figura 1).
Referências
1. RSC: Enterprise and electrolysis, consultado em 02/03/2010.
2. Online Etymology Dictionary: electrolysis, consultado em 02/03/2010.
Criada em 27 de Março de 2010
Revista em 14 de Dezembro de 2010
Aceite pelo editor em 14 de Dezembro de 2010