Álcool contra a COVID-19
Referência : Ramos, M.J., Fernandes, P.A., (2020) O álcool contra a COVID-19, Rev. Ciência Elem., V8(2):018
Autores: Maria João Ramos e Pedro Alexandrino Fernandes
Editor: José Ferreira Gomes
DOI: [http://doi.org/10.24927/rce2020.018]

Durante a pandemia da COVID-19, foram recomendados dois meios de desinfeção do vírus SARS-CoV-2, a repetida lavagem com sabão e o álcool a 60% ou mais. O uso do álcool não causa surpresa porque estamos habituados a usá-lo como meio geral de desinfeção, mas interessa compreender o seu mecanismo de ação. O efeito baseia-se na desnaturação de glicoproteínas que fazem parte do envelope do vírus, sendo que a desnaturação as impede de exercerem as suas funções biológicas, químicas e físicas.
Embora o sabão seja o agente mais eficiente para a inativação do SARS-CoV-2, o vírus causador da COVID-19, o que podemos fazer se não tivermos água e sabão disponíveis para lavar as mãos? A resposta está em que desinfetantes, géis, cremes, toalhetes e líquidos que contenham um mínimo de 60% de álcool, são também muito úteis para a inativação do vírus. Os álcoois mais utilizados nos desinfetantes etc, são o etanol, o propanol e o isopropanol (o segundo menos utilizado do que os outros dois, ver FIGURA 1).
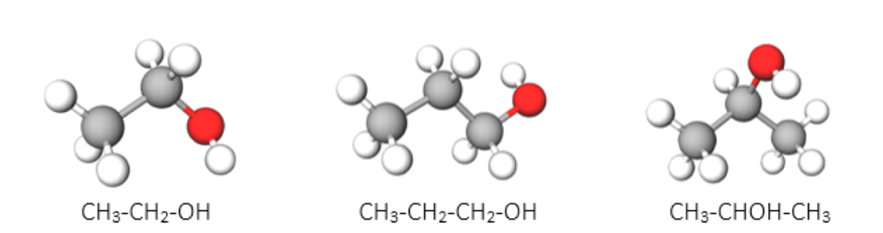
Estes álcoois são eficazes na inativação da maioria dos vírus embora existam alguns tipos de vírus que eles não conseguem destruir. Estes últimos são vírus que possuem uma forte camada proteica que protege o seu material genético. Os outros são vírus que possuem, adicionalmente, um envelope viral, i.e. uma membrana constituída por uma bicamada de fosfolípidos e proteínas associadas, a proteger o seu material genético. Assim, vírus não envelopados, como seja o norovírus (um vírus extremamente contagioso que provoca vómitos e diarreia), não são inativados por álcoois. No entanto, o SARS-CoV-2 é um vírus envelopado, e esse mesmo envelope viral resulta num dos possíveis alvos para o destruir, tornando este tipo de vírus o mais vulnerável e fácil de inativar. Os coronavírus têm sobrevivência limitada fora dos ambientes hospedeiros e, geralmente, transferem-se diretamente de hospedeiro para hospedeiro. Os vírus envelopados possuem grande adaptabilidade e podem mutar em pouco tempo para evitar o sistema imunológico humano, podendo causar infeções persistentes.
O envelope viral é muito sensível aos álcoois. Vamos ver porquê...
Enrolamento proteico
As glicoproteínas virais, existentes na superfície do envelope, servem para identificar os recetores na membrana do hospedeiro e para se ligarem aos mesmos. A entrada do SARS-CoV-2 nas células hospedeiras é mediada pela glicoproteína S (do inglês spike), resultando num processo complexo para promover a fusão célula-vírus. Eventualmente, o envelope viral funde-se com a membrana do hospedeiro, permitindo que a cápside e o genoma viral entrem e infetem o hospedeiro.
Ora, todas as proteínas, incluindo a glicoproteína S, têm uma determinada estrutura que obedece a um enrolamento proteico característico de cada uma delas, a chamada estrutura terciária da proteína. O enrolamento proteico é o processo físico pelo qual a proteína adota uma conformação biologicamente funcional, que corresponde à sua estrutura tridimensional nativa (FIGURA 2). O enrolamento proteico é um processo muito complexo ocorrendo, de um modo geral, na escala do milissegundo.
A tradução de uma sequência do ARN mensageiro (mARN) para uma cadeia de aminoácidos transforma as proteínas em cadeias de polipéptidos, sem estrutura tridimensional estável. O enrolamento proteico começa a ocorrer ainda durante a tradução da cadeia polipeptídica, os aminoácidos interagem entre si e o processo resulta numa estrutura tridimensional bem definida – a proteína nativa.
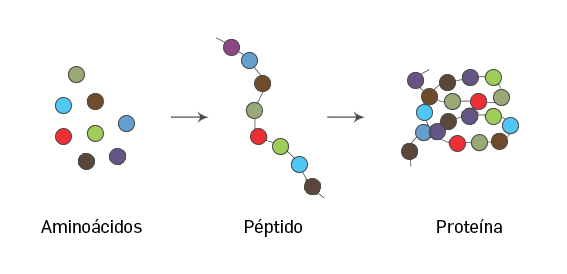
Existem atualmente diversas técnicas que ajudam a estudar o enrolamento de proteínas nomeadamente, entre outras, a ressonância magnética nuclear (RMN), o dicroísmo circular (DC), a cristalografia de raios-x, a microscopia de força atómica (MFA) e a modelação molecular computacional que é, neste momento, excecional para capturar a dinâmica do processo de enrolamento proteico.
A estrutura tridimensional correta é essencial para o bom funcionamento da proteína. Se por algum motivo, a desnaturação da proteína ocorrer, i.e. basicamente o processo inverso do enrolamento proteico, as propriedades biológicas, químicas e físicas são alteradas devido a perturbações causadas na sua estrutura tridimensional, e o reconhecimento molecular para essa proteína deixa de funcionar.
Reconhecimento molecular
A glicoproteína S, do SARS-CoV-2, interage diretamente com a enzima conversora de angiotensina 2 (hACE2) humana, ligando-se à mesma com uma afinidade elevada, entrando, deste modo, na célula do hospedeiro.
Faz-se aqui uma pequena referência à enzima hACE2 - é uma enzima ligada à superfície externa das células nos pulmões, artérias, coração, rins e intestino. Esta enzima reduz a pressão sanguínea catalisando a clivagem da angiotensina II (um vasoconstritor) em angiotensina (um vasodilatador). A hACE2 serve como ponto de entrada de alguns coronavírus, nomeadamente do SARS-CoV-2.
Na realidade, cada proteína se liga ao recetor respetivo de um modo específico. A esta interação específica entre moléculas, exibindo complementaridade molecular através de ligações não covalentes como, por exemplo, ligações de hidrogénio, forças de van der Waals ou forças eletrostáticas, chama-se reconhecimento molecular. Como exemplo concreto de reconhecimento molecular, a FIGURA 3 apresenta uma representação esquemática da estrutura tridimensional da glicoproteína S do vírus SARS-CoV-2 ligada à enzima hACE2.
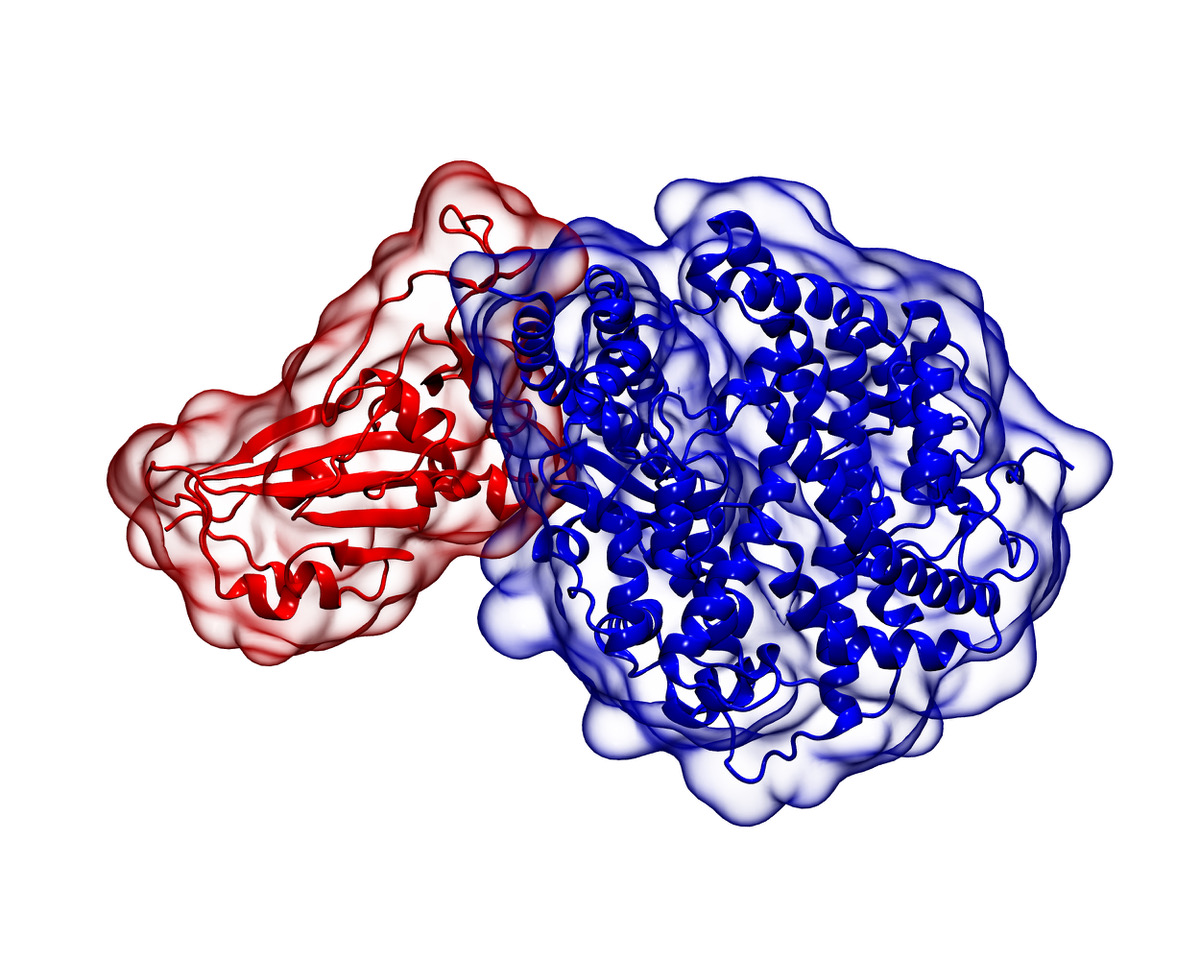
Os álcoois são eficazes para inativar o vírus porque eles atuam na estrutura da glicoproteína S, desnaturando-a, ou seja, como referido anteriormente, alterando as suas propriedades biológicas, químicas e físicas devido a perturbações causadas na sua estrutura terciária. De um modo geral, a adição de álcoois melhora as interações polares locais nas proteínas e enfraquece as interações hidrofóbicas não locais. Isso resulta na desestabilização dos núcleos hidrofóbicos nativos das proteínas e no aumento da formação de ligações locais de hidrogénio álcool-proteína, resultando em proteínas desnaturadas. A ramificação da cadeia do álcool tende a reduzir a sua capacidade de desnaturação das proteínas.
Em conclusão, o vírus SARS-CoV-2, causador da COVID-19, é um agente patogénico novo cuja proteína S se liga com afinidade elevada à enzima humana ACE2, hACE2, usando-a como um recetor de entrada para invadir a célula do hospedeiro, neste caso o ser humano. Os álcoois provocam a desnaturação da proteína S do vírus impedindo-a, assim, de efetuar o reconhecimento molecular da enzima hACE2 e, consequentemente, impedindo a entrada do vírus na célula humana.
Fatores importantes
O sabão continua a ser o agente mais eficiente para inativar o vírus causador da COVID-19. Atualmente, no entanto, existem também desinfetantes à base de álcool, geralmente contendo etanol. Outros álcoois também usados são o propanol e o isopropanol.
É importante a consideração de alguns fatores:
- De um modo geral, os desinfetantes para as mãos à base de álcool contêm entre 60 a 95% (em volume) de álcool. A potência dos desinfetantes para as mãos à base de álcool aumenta com a percentagem em volume de álcool. No entanto, concentrações em álcool muito elevadas (acima de 95%) são menos eficazes. Isso ocorre porque as proteínas não são tão facilmente desnaturadas em ambientes hidrofóbicos, ou seja, em ambientes desprovidos de água.
- É necessário que o volume de desinfetante utilizado seja suficiente para cobrir toda a área de ambas as mãos. Caso contrário, haverá áreas onde o vírus continuará a existir. Para cobrir adequadamente ambas as mãos, é necessário usar cerca de 3 ml de desinfetante (aproximadamente uma palma da mão).
- Se as mãos estiverem cobertas de sujidade ou gordura, o desinfetante para as mãos não as consegue remover. Deste modo, o vírus pode permanecer nas mãos sujas.
Com todas estas advertências, é fácil de entender por que é que as recomendações habitualmente dadas, se concentram na lavagem das mãos. Na realidade, se lavarmos as mãos pelo período de 20 segundos recomendado, toda a sujidade, gordura e vírus (e bactérias também) serão removidos!
[editar] Referências
- LAN, J. et al. Structure of the SARS-CoV-2 spike receptor-binding domain bound to the ACE2 receptor, Nature. 2020
- WANG, Q. et al. Structural and Functional Basis of SARS-CoV-2 Entry by Using Human ACE2, Cell 181, 1–11, 2020.
Recursos relacionados disponíveis na Casa das Ciências:
Criada em 16 de Abril de 2020
Revista em 20 de Abril de 2020
Aceite pelo editor em 21 de Abril de 2020

