Ácidos Gordos
Referência : Gesto, D., (2014) Ácidos Gordos, Rev. Ciência Elem., V2(4):278
Autor: Diana Gesto
Editor: Pedro Alexandrino Fernandes
DOI: [http://doi.org/10.24927/rce2014.278]

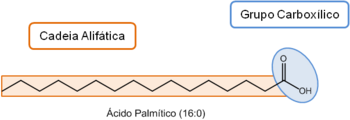
Os ácidos gordos são derivados de hidrocarbonetos compostos por uma longa cadeia alifática não ramificada e por um grupo carboxílico. Tal como a glicose, os ácidos gordos são uma importante fonte de energia para as células, sendo estes armazenados no tecido adiposo sob a forma de triglicerídeos. Estes são também um dos precursores dos fosfolípidos e muitos outros lípidos com diversas funções. Se os ácidos gordos não estiverem associados a mais nenhuma molécula são designados por ácidos gordos livres.
A cadeia alifática dos ácidos gordos pode variar entre 4 e 36 carbonos. No entanto, nas células, os ácidos gordos predominantes apresentam um número par de átomos de carbonos, geralmente 14, 16, 18 ou 20. Os ácidos gordos podem ser classificados como saturados ou insaturados, dependendo da presença ou não de ligações duplas C-C na cadeia alifática. Assim, se um determinado ácido gordo apresentar uma ou mais ligações duplas, este será classificado como insaturado ou poli-insaturado (se tiver mais que uma), enquanto que um que não apresente qualquer ligação dupla será saturado.
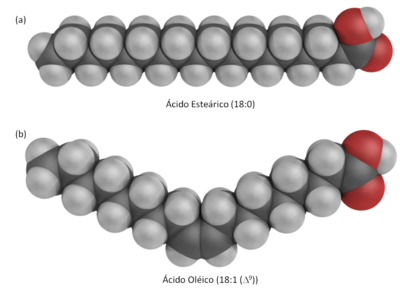
Uma das nomenclaturas mais simples e usuais para designar ácidos gordos utiliza abreviaturas do tipo X:Y, em que X designa o número de carbonos da molécula e Y o número de ligações duplas. Desta forma, uma molécula composta por 14 carbonos (incluindo o do grupo carboxílico) e sem ligações duplas seria designada por 14:0. Caso existam ligações duplas, pode ainda especificar-se a sua localização utilizando o símbolo Δ(delta). Assim, um ácido gordo com 18 carbonos e duas ligações duplas, uma entre o C-9 e o C-10 e outra entre o C-12 e C-13 (sendo C-1 o carbono do grupo carboxílico) é designado 18:2(Δ9,12).
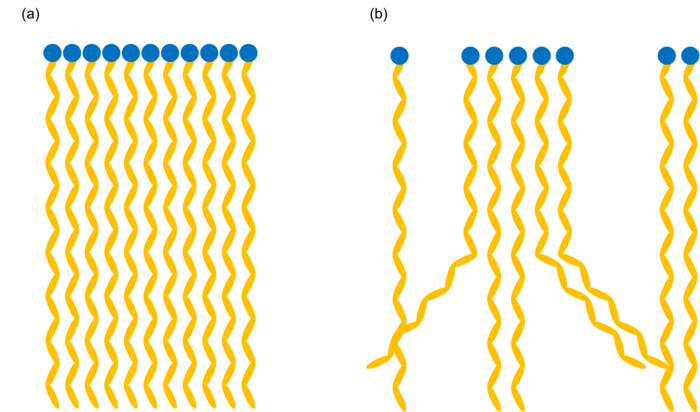
As propriedades físicas dos ácidos gordos são maioritariamente determinadas pelo tamanho da cadeia alifática e pelo número de ligações duplas. Apesar de possuírem um grupo hidrofílico na sua constituição, a maioria dos ácidos gordos são insolúveis em água, devido à cadeia de carbonos, e quanto maior esta cadeia for e menor número de ligações duplas tiver, menor será também a sua solubilidade. A temperatura de fusão varia de forma semelhante mas inversa: quanto maior for a cadeia e menor for o número de ligações duplas, maior é a temperatura de fusão. A razão para este comportamento prende-se com o empacotamento das moléculas. A cadeia alifática dos ácidos gordos saturados é praticamente linear e bastante mais flexível do que cadeias que apresentem ligações duplas, o que permite que as moléculas se disponham de maneira a maximizar o número de interacções dispersivas. Assim, quanto maior o número de interacções entre as moléculas será necessário fornecer também mais energia ao sistema para quebrar estas ligações, o que se traduz num aumento do ponto de fusão. No caso dos ácidos gordos insaturados, a presença de uma ligação dupla leva a uma torção na cadeia, o que dificulta o empacotamento, e desta forma, as interacções entre as moléculas são mais fracas.
Referências
A. Lehninger, D. Nelson, M. Cox, Lehninger principles of biochemistry , Fifth Edition, W.H. Freeman: New York, 2008, ISBN: 9780716771081.
Harvey F. Lodish, Molecular cell biology, Fifth Edition, W. H. Freeman: New York, 2004, ISBN: 0716743663.
Criada em 12 de Janeiro de 2011
Revista em 19 de Janeiro de 2011
Aceite pelo editor em 19 de Janeiro de 2011