Nanomateriais híbridos de ouro/sílica
Referência : Martins, F., Pereira, E., Pereira, C. R., (2023) Nanomateriais híbridos de ouro/sílica, Rev. Ciência Elem., V11(3):034
Autora: Fábio Martins, Eulália Pereira e Clara R. Pereira
Editor: João Nuno Tavares
DOI: [https://doi.org/10.24927/rce2023.034]

[editar] Resumo
As nanopartículas de ouro e de sílica têm aplicação em diversas áreas da ciência e tecnologia devido às suas propriedades únicas e à sua versatilidade. O desenvolvimento de nanomateriais híbridos de ouro/sílica tem assumido especial destaque e aberto novos campos de oportunidades, devido à conjugação das propriedades de ambos os componentes num único nanomaterial (multifuncionalidade) e surgimento de novas propriedades sinérgicas. O presente artigo incide sobre esta classe de nanomateriais híbridos. Primeiramente, apresenta-se uma perspetiva histórica e as propriedades únicas dos nanomateriais híbridos de ouro/sílica, seguindo-se alguns dos métodos mais relevantes usados para a sua preparação. Por último, apresentam-se alguns exemplos de aplicações atuais de nanomateriais híbridos de ouro/sílica, nomeadamente no tratamento do cancro e na purificação de águas.
Antes de introduzir a classe de nanomateriais híbridos de ouro/sílica, é importante começar por definir alguns conceitos fundamentais, nomeadamente o que são nanomateriais e o que distingue nanomateriais híbridos de nanomateriais constituídos por um único componente. Segundo a União Internacional de Química Pura e Aplicada (IUPAC), uma nanopartícula é definida como sendo uma partícula que apresenta pelo menos uma das suas dimensões entre 1 e 100 nm. A escolha deste limite superior baseia-se no facto destas partículas apresentarem propriedades distintas das propriedades do mesmo material macroscópico (bulk material). Contudo, o termo “nano” pode ainda ser estendido a materiais com dimensões inferiores a 500 nm, quando estes apresentam propriedades diferentes dos materiais macroscópicos correspondentes, nomeadamente propriedades químicas, elétricas, óticas, mecânicas, magnéticas e reológicas[1].
As propriedades únicas de nanomateriais constituídos por um único componente, por exemplo, nanopartículas de ouro, nanopartículas de sílica e nanomateriais de óxidos de ferro magnéticos, levou ao desenvolvimento de métodos para a sua síntese que permitam obter um elevado controlo de parâmetros como a morfologia (tamanho e forma), propriedades texturais (área superficial específica e porosidade) e química superficial. Nas últimas décadas, tem-se observado um interesse crescente na investigação e desenvolvimento de sistemas substancialmente mais complexos, constituídos por pelo menos dois nanomateriais diferentes, os quais são designados de nanomateriais híbridos[2]. Estes novos materiais permitem não só ultrapassar algumas das limitações inerentes aos nanomateriais monocomponente, mas também apresentam novas propriedades provenientes da interação entre os componentes, permitindo assim desenvolver plataformas multifuncionais.
Recentemente, os nanomateriais híbridos de ouro e sílica têm suscitado um especial interesse para diversas aplicações, nomeadamente nas áreas da biomedicina[3], [4], [5], [6], [7], [8], [9], desenvolvimento de sensores para quantificação de espécies químicas[10], [11] e catálise[12], [13], [14], [15]. Este artigo apresenta uma perspetiva abrangente sobre os nanomateriais híbridos de ouro/sílica e sua importância na atualidade. Na primeira parte apresenta-se um breve enquadramento histórico, seguido de uma discussão sobre as suas principais propriedades e métodos de síntese. Por último, serão apresentados alguns exemplos atuais de aplicações deste tipo de nanomateriais, assim como conclusões e perspetivas futuras desta área de investigação.
Perspetiva histórica.
O início da nanotecnologia é muitas vezes conotado com a famosa palestra do físico Richard Feynman, em 1959, intitulada There’s Plenty of Room at the Bottom[16]. No entanto, nessa altura, as capacidades técnicas de miniaturização eram muito limitadas, pelo que a proposta de Feynman era ainda meramente especulativa. Só a partir da década de 1970 é que verdadeiramente se iniciou a investigação científica em nanotecnologia, possibilitada pelos avanços nas técnicas de miniaturização e de microscopia. A área foi batizada por Norio Taniguchi, em 1974[17], e teve como um dos seus grandes ideólogos o físico Eric Drexler, que despoletou um elevado interesse na comunidade científica e na opinião pública com a publicação do livro Engines of Creation: The Coming Era of Nanotechnology, em 1986[18].
A história dos materiais componentes dos híbridos em que nos focamos neste artigo, o ouro e a sílica, é bem mais antiga, com várias aplicações tecnológicas reportadas ao longo da história da humanidade. Além da sua utilização em joalharia, o ouro, quer à macroescala quer à nanoescala (nanopartículas), foi utilizado em medicina e na produção de vidro dicroico (FIGURA 1).

Na Idade Média, os elixires de ouro eram um remédio para o tratamento de febres e até mesmo da sífilis. Contudo, só em 1890 é que a sua utilização foi reportada na medicina moderna pelo bacterologista Robert Koch, que identificou os efeitos tóxicos do ouro no tratamento da tuberculose[20], [21], [22]. Embora ainda se possam encontrar terapias análogas, com o desenvolvimento da medicina moderna, muitas destas têm caído em desuso.
A sílica existe na natureza sob a forma de quartzo, o segundo mineral mais abundante na crosta terrestre, sendo utilizada desde a pré-história no fabrico de utensílios, armas e objetos decorativos. Hoje em dia, continua a ser uma matéria prima muito importante na indústria da construção, fabrico do vidro, indústria eletrónica e nas indústrias alimentar, farmacêutica e cosmética. A sua utilização sob a forma de nanopartículas começou na década de 1970, após a descoberta do processo de síntese por Werner Stöber em 1968[23]. Nos anos que se sucederam, foram propostas diversas otimizações e aprimoramentos ao método de Stöber, dando origem a nanomateriais de sílica com novas morfologias e propriedades texturais[24]. Em particular, destaca-se a introdução de porosidade na estrutura da sílica, produzindo assim sílica mesoporosa, com aplicações em catálise, entrega controlada de fármacos e imagiologia.
Propriedades das nanopartículas de ouro e das nanopartículas de sílica.
As nanopartículas de ouro e de sílica por si só apresentam um conjunto considerável de propriedades apelativas. As nanopartículas de ouro têm uma elevada estabilidade química e coloidal, assim como uma baixa toxicidade, o que as torna perfeitas para aplicações biológicas[25], [26], [27], [28]. No entanto, são as suas propriedades óticas únicas que as tornam tão interessantes para inúmeras aplicações tecnológicas. Estas propriedades óticas advêm da forma como as nanopartículas de ouro interagem com a radiação eletromagnética. Quando a radiação eletromagnética incide sobre um metal, o campo eletromagnético oscilante da luz induz a oscilação da nuvem eletrónica de condução na superfície da partícula. À escala nanométrica esse fenómeno, denominado de ressonância plasmónica de superfície localizada, dá origem a uma forte absorção de radiação eletromagnética (FIGURA 2).
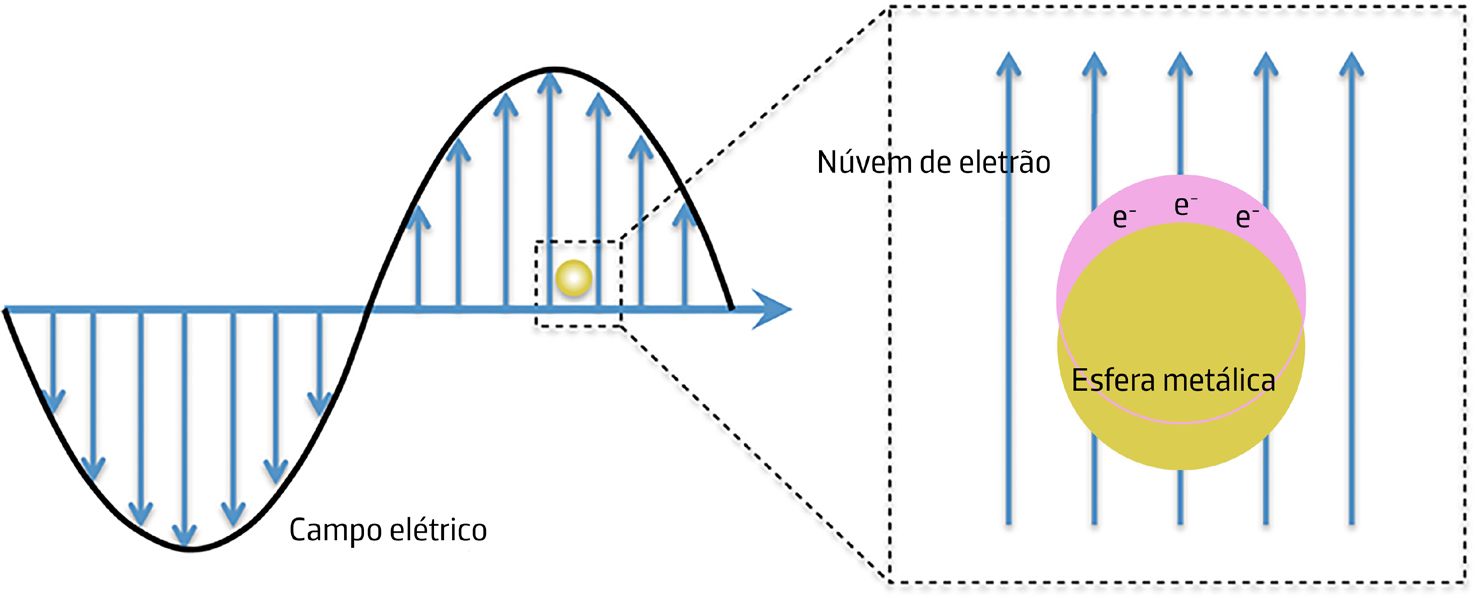
Tal ocorre quando a frequência da radiação incidente iguala a frequência de oscilação natural dos eletrões à superfície da nanopartícula, dando origem a uma interação construtiva. Este fenómeno é responsável pela absorção de energia que, por sua vez, pode dar origem a dispersão de radiação, conversão em calor ou transferência para moléculas na proximidade da superfície da partícula, isto é, espécies químicas que se encontrem ancoradas ou adsorvidas na sua superfície.
No caso das nanopartículas de ouro, a banda plasmónica de superfície localizada ocorre a um comprimento de onda na região do visível, propriedade que partilha apenas com dois outros metais, a prata e o cobre. A frequência de ressonância plasmónica de superfície localizada depende de vários fatores, nomeadamente do tamanho e forma das nanopartículas, assim como da constante dielétrica do meio circundante. Por exemplo, as nanopartículas de ouro esféricas com cerca de 15 a 20 nm de diâmetro apresentam uma cor vermelha devido a fenómenos de ressonância a um comprimento de onda de 520 nm. Para nanopartículas esféricas de dimensões superiores, o comprimento de onda a que ocorre a ressonância aumenta, levando progressivamente a uma cor mais arroxeada (FIGURA 3). A variação de cor é ainda mais drástica para nanopartículas não esféricas. No entanto, a propriedade mais relevante destas bandas de absorção é a sua elevada intensidade, com coeficientes de extinção que podem ser até 1000 vezes superiores aos de corantes orgânicos.

Similarmente às nanopartículas de ouro, as nanopartículas de sílica possuem uma elevada estabilidade química e coloidal e baixa toxicidade, permitindo assim a sua utilização em aplicações biológicas. Contudo, o grande trunfo das nanopartículas de sílica é a possibilidade de, no processo de síntese, conferir-lhes uma estrutura com elevada porosidade e área superficial[30]. Esta característica das sílicas porosas, especialmente das sílicas mesoporosas (tamanho de poro entre 2 e 50 nm), faz deste tipo de partículas excelentes plataformas para introdução de espécies químicas, quer para utilização como nano-reatores, quer para a entrega controlada de fármacos[31], [32], [33], [34]. As nanopartículas de sílica também apresentam uma química superficial muito rica, devido à presença de grupos silanol, o que permite a ligação de moléculas orgânicas e a sua hibridização com outros nanomateriais.
As propriedades singulares destas duas famílias de nanomateriais podem ser facilmente combinadas numa só plataforma, através da preparação de nanopartículas híbridas de ouro/sílica[35], [36], [37], [38], [39], [40], [41]. Dessa forma é possível conjugar as propriedades óticas do ouro, com a elevada área superficial da sílica mesoporosa, mantendo ainda uma excelente biocompatibilidade e estabilidade. Esta multifuncionalidade pode ser útil numa vasta gama de aplicações, desde a construção de sensores para deteção e quantificação de espécies químicas/ bioquímicas, à remoção de poluentes existentes em águas residuais e, até mesmo, ao diagnóstico e tratamento de doenças.
Preparação de nanomateriais híbridos de ouro/sílica.
A preparação de nanomateriais híbridos tem sido um dos grandes desafios em nanotecnologia, dado que a conjugação de materiais diferentes exige que se ultrapasse o problema da incompatibilidade existente entre a estrutura cristalina de diversos materiais e, em muitos casos, da sua baixa adesão. Atualmente, são já conhecidas diversas estratégias de síntese que permitem preparar materiais híbridos com um excelente controlo do seu tamanho/distribuição de tamanhos, forma e química de superfície. Em nanopartículas híbridas, a conformação relativa entre os dois componentes dá origem a diferentes tipos de partículas, destacando-se (FIGURA 4)[42], [43]: A) Nanopartículas núcleo-coroa (core-shell); B) Nanopartículas tipo saco vitelino (yolk-shell); C) Nanopartículas heterodiméricas; D) Nanopartículas de Janus; E) Nanopartículas decoradas. Nesta secção serão somente abordados os processos de síntese mais relevantes para a preparação de nanopartículas híbridas de ouro/sílica de três tipos, nomeadamente núcleo-coroa, nanopartículas de Janus e nanopartículas decoradas.
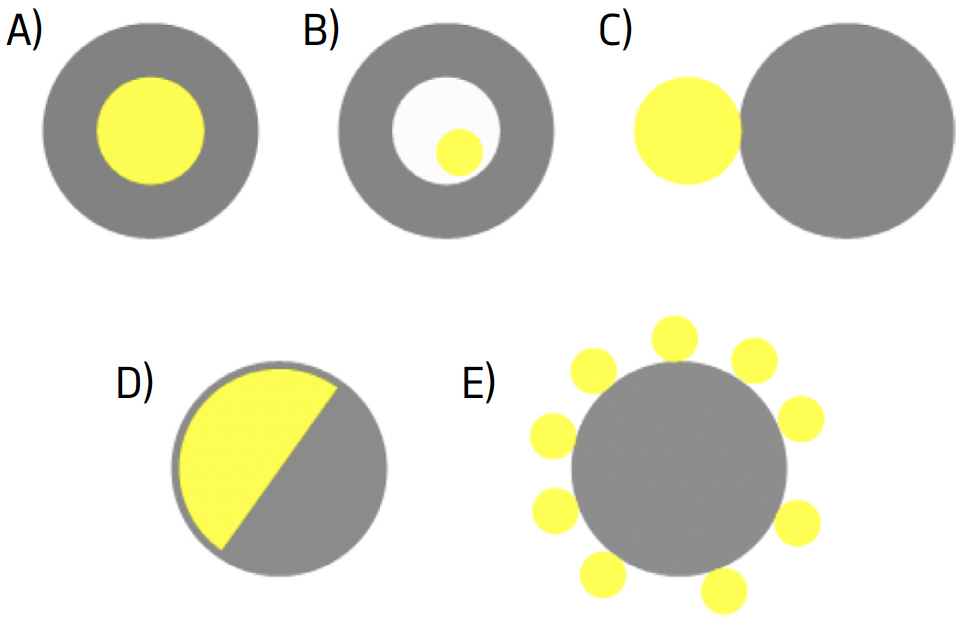
Nanopartículas núcleo-coroa.
De entre os diversos tipos de nano-estruturas mencionados anteriormente, as mais estudadas são as nanopartículas núcleo-coroa. A estratégia de síntese usual ocorre em duas etapas: uma primeira etapa onde se preparam as nanopartículas que vão formar o núcleo e uma segunda etapa de revestimento do núcleo com outro material, que forma a coroa da nanopartícula[44]. As propriedades dos nanomateriais híbridos núcleo-coroa podem ser ajustadas através de variações estruturais e morfológicas, nomeadamente alteração do número de núcleos revestidos pela coroa, tamanho dos núcleos, espessura da coroa, número de camadas de revestimento, entre outras[45], [46], [47], [48], [49], [50]. A estratégia mais comum é a criação de nanopartículas mononucleares, com núcleo de ouro e coroa de sílica, tipicamente sílica mesoporosa.
Para a primeira etapa de preparação dos núcleos de ouro pode utilizar-se qualquer dos inúmeros métodos de síntese de nanopartículas de ouro, nomeadamente com forma esférica, de estrela, de bastonete, entre muitas outras[51], [52]. O método mais usado é uma adaptação do processo publicado por Turkevich e co-autores, em 1951, para a preparação de nanopartículas esféricas de ouro, com um diâmetro de cerca de 15 nm[53]. Este método baseia-se na redução de um precursor de ouro(III) com citrato de sódio. O anião citrato também funciona como um estabilizador coloidal (agente de revestimento). São conhecidos outros métodos semelhantes usando outros redutores químicos e outros agentes de revestimento que, consoante a sua natureza, podem originar partículas com outras morfologias[54], [55], [56], [57], [58]. Por exemplo, a utilização de brometo de hexadeciltrimetilamónio (CTAB) como agente de revestimento leva à formação de nanobastonetes de ouro.
Para a segunda etapa de revestimento com sílica usa-se habitualmente o método de Stöber (método sol-gel)[59], que se baseia na ocorrência de reações de hidrólise e de condensação de um precursor de sílica, tipicamente o tetraetilortossilicato (TEOS), em meio básico[60], [61], [62] (FIGURA 5). A formação da coroa de sílica pode ser favorecida relativamente à formação de nanopartículas de sílica puras, utilizando um agente de revestimento do núcleo de ouro bifuncional (por exemplo, um organossilano), tal como o apresentado na FIGURA 5. Este agente adsorve fortemente às nanopartículas de ouro através do grupo X, usualmente um grupo amina ou tiol e, na extremidade voltada para o exterior, contém um grupo silanol ou alcoxilo, adequado para condensação com o TEOS.
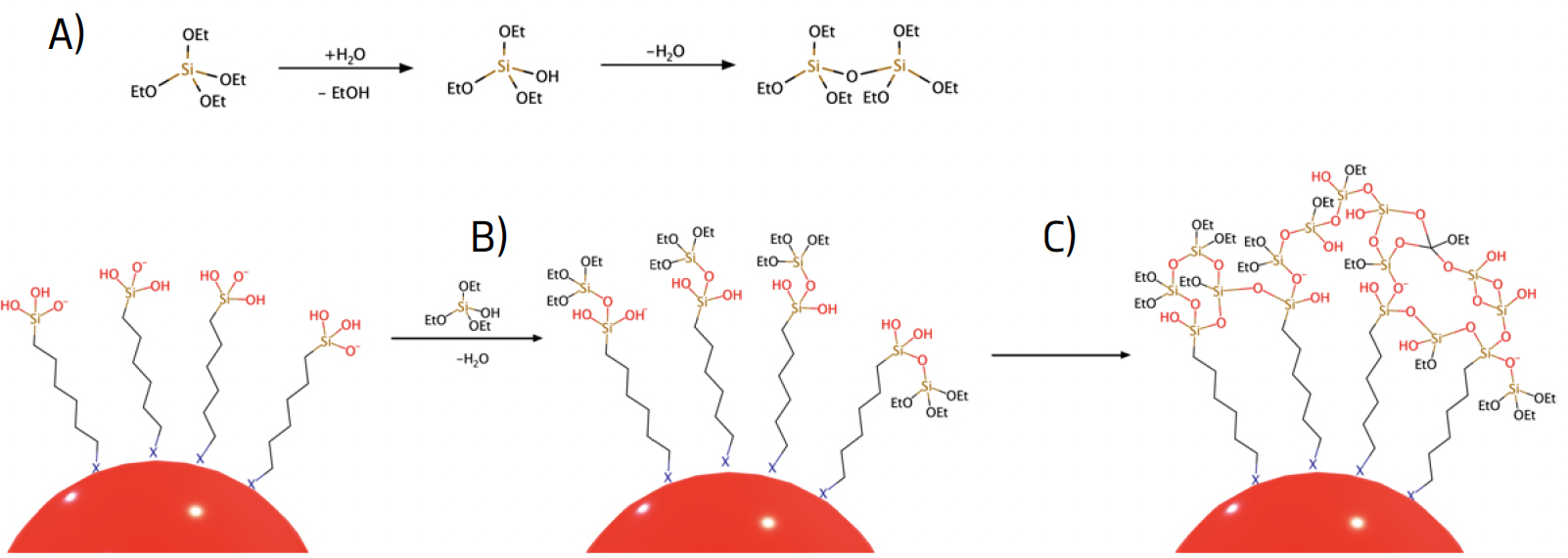
A reação também pode ser realizada na presença de um surfactante capaz de produzir micelas cilíndricas (por exemplo, o CTAB), que é utilizado como molde para a criação de poros no revestimento de sílica, criando assim sílica mesoporosa. A natureza e a concentração do surfactante permitem controlar a morfologia das micelas que, por sua vez, governarão a forma e tamanho dos poros[63].
Nanopartículas de Janus.
As nanopartículas de Janus são outro tipo de nanoestruturas em que o núcleo se encontra apenas parcialmente revestido. O revestimento parcial resolve um dos grandes problemas das nanopartículas núcleo-coroa de ouro/sílica relativo à perda das propriedades óticas do núcleo de ouro com o aumento de espessura da coroa de sílica. Tal como foi demonstrado por Park e co-autores[64], mantendo parte da nanopartícula de ouro exposta assegura-se a manutenção das propriedades óticas do ouro, ao mesmo tempo que se preserva a estabilidade coloidal proporcionada pelo revestimento de sílica.
Conhecem-se várias estratégias de síntese de nanopartículas de Janus baseadas na proteção de parte da nanopartícula de ouro relativamente à formação da coroa de sílica. Tal exige que o núcleo de ouro tenha uma superfície anisotrópica que permita um revestimento não uniforme da superfície. Por exemplo, outros autores recorreram às propriedades de segregação de dois agentes de revestimento, o ácido poliacrílico (PAA) e o ácido 4-mercaptobenzóico (4- MBA), na superfície de nanopartículas de ouro[65]. Esta segregação leva a que parte da superfície da nanopartícula fique revestida por 4-MBA e a restante superfície revestida por PAA. Uma vez que o PAA pode inibir a reação de condensação do TEOS, o revestimento de sílica só se forma nas regiões cobertas por 4-MBA. Através do controlo entre a proporção de PAA e 4-MBA é possível obter partículas com vários graus de cobertura com sílica.
Nanopartículas decoradas.
As nanopartículas de sílica decoradas com ouro são formadas através da deposição de partículas pequenas de ouro na superfície da sílica. Estas nanopartículas podem ser sintetizadas através da redução in situ de um precursor de ouro(III) na superfície da nanopartícula de sílica[66], [67], [68]. No caso de nanopartículas de sílica mesoporosas, a redução do ouro(III) pode ocorrer em três locais distintos: à superfície da sílica, nos poros das partículas e no meio reacional. Uma vez que o principal objetivo consiste na deposição exclusiva de nanopartículas de ouro na superfície da sílica, o controlo do local onde ocorre a redução do precursor de ouro é crucial. O método mais comum para decorar nanopartículas de sílica com ouro baseia-se na funcionalização de nanopartículas de sílica com grupos funcionais amina (–NH2), seguida da adsorção de um precursor de ouro aniónico e posterior redução a ouro metálico. Desta forma, a pH acídico, os grupos amina carregados positivamente irão atrair o precursor de ouro carregado negativamente, levando assim à sua adsorção à superfície da sílica, onde serão posteriormente reduzidos a ouro metálico. Uma estratégia alternativa consiste na formação de ligações covalentes entre grupos funcionais presentes na superfície das nanopartículas de sílica e de ouro. No entanto, essas ligações poderão ser sensíveis a estímulos externos, como é o caso de aplicações em entrega de fármacos.
Aplicações.
Os nanomateriais de ouro/sílica têm sido utilizados nas mais diversas áreas da ciência e tecnologia, com especial destaque para catálise, produção de sensores químicos e bioquímicos, técnicas de imagiologia, tratamento do cancro, entre outros[69], [70], [71], [72], [73], [74], [75], [76], [77], [78], [79], [80], [81], [82], [83], [84], . Nesta secção serão apresentadas apenas duas destas aplicações, nomeadamente na purificação de água e na entrega controlada de fármacos para o tratamento do cancro.
Aplicação na purificação de água.
A escassez de recursos hídricos devido à poluição e ao aquecimento global tem atingido um nível muito preocupante, mesmo em regiões com climas moderados. Assim, são necessários novos métodos que permitam purificar água de um modo eficaz e energeticamente eficiente, tal como reconhecido nos Objetivos de Desenvolvimento Sustentável da Organização das Nações Unidas (ONU)[85]. Uma das soluções energeticamente favoráveis consiste na utilização de nanopartículas de ouro na purificação de água por evaporação. Esta estratégia baseia-se na excelente conversão fototérmica das nanopartículas de ouro devido à ressonância plasmónica de superfície localizada. Contudo, a aplicação desta tecnologia em grande escala pode não ser sustentável, devido ao elevado custo do ouro e também à sua baixa disponibilidade. Para resolver este problema, Cui e co-autores desenvolveram uma membrana contendo microesferas de sílica funcionalizadas com nanopartículas de ouro[86]. Estas nanopartículas mantêm as propriedades de conversão fototérmica do ouro mas utilizando uma quantidade de ouro substancialmente inferior. O sistema proposto permite a remoção de sais e de outros contaminantes por evaporação da água do mar, utilizando o aquecimento do material híbrido exposto à luz solar.
Aplicação em entrega controlada de fármacos.
A entrega controlada de fármacos é outra área onde as nanopartículas híbridas de ouro e sílica têm sido utilizadas. A elevada área superficial da sílica mesoporosa permite o transporte de elevadas cargas de fármacos, protegendo-os de fenómenos de degradação e eliminação. Por seu lado, a componente de ouro permite gerar um estímulo térmico no local alvo para que o fármaco seja libertado somente nesse local. É precisamente deste modo que a nanoplataforma proposta por Cheng e co-autores funciona[87]. A estratégia da preparação da nanoplataforma começou com a incorporação de doxorubicina, um agente quimioterapêutico para o tratamento de vários tipos de cancro, em sílica mesoporosa. Seguidamente, funcionalizaram-se as nanopartículas de sílica com nanopartículas de ouro, que bloqueiam os poros da sílica, prevenindo assim a libertação do fármaco. A libertação do fármaco no local alvo foi efetuada por irradiação de infravermelho próximo (NIR), provocando aquecimento local e abertura dos poros. Além da libertação controlada do fármaco, as nanoplataformas permitem um aquecimento local do tumor, o que potencia o efeito citotóxico do agente quimioterapêutico, bem como desencadeia vários mecanismos de morte das células cancerígenas. Deste modo, este nanomaterial, além de proporcionar uma entrega controlada do fármaco no local alvo, diminuindo os efeitos secundários da quimioterapia, combina duas terapias de combate ao cancro, nomeadamente, a quimioterapia e a termoterapia, aumentando assim a eficácia do tratamento.
Conclusões e perspetivas futuras.
As nanopartículas híbridas de ouro/sílica apresentam um grande potencial comparativamente aos nanomateriais monocomponente que as constituem. A hibridização de nanopartículas de ouro e de sílica permite desenvolver nanomateriais multifuncionais que conjugam as propriedades óticas e fototérmicas únicas do ouro com a porosidade finamente controlada, química superficial e estabilidade coloidal da nano-sílica. Por outro lado, permitem solucionar algumas das principais limitações intrínsecas a cada um dos materiais individualmente, nomeadamente aumentar a estabilidade coloidal, minimizar a agregação dos núcleos de ouro e conferir maior proteção das suas propriedades óticas. Esta família de nanomateriais multifuncionais permite assim desenvolver estratégias únicas como a abordada para o tratamento do cancro que apenas pode ser obtida pela conjugação entre estes dois materiais.
Contudo, é de realçar que esta ainda é uma área em desenvolvimento e que certamente, num futuro próximo, será possível beneficiar da sua aplicação em métodos avançados de diagnóstico e tratamento de doenças (teragnóstico), assim como na sua utilização como nano-reatores com propriedades catalíticas importantes para a degradação de poluentes. De tal forma é de esperar um futuro brilhante para esta classe extraordinária de nanomateriais híbridos.
Agradecimentos.
Clara R. Pereira agradece à Fundação para a Ciência e a Tecnologia pelo financiamento no âmbito do Concurso de Estímulo ao Emprego Científico Individual– CEEC Individual (Ref. 2021.04120.CEECIND/CP1662/CT0008).
[editar] Referências
- ↑ VERT, M. et al., Terminology for Biorelated Polymers and Applications (IUPAC Recommendations 2012), Pure Appl. Chem., 84, 377. 2012.
- ↑ MA, D., Chapter 1 - Hybrid Nanoparticles: An Introduction, em Noble Metal-Metal Oxide Hybrid Nanoparticles: Fundamentals and Applications, Noble Metal-Metal Oxide Hybrid Nanoparticles Fundamentals and Applications, Micro and Nano Technologies, Elsevier, 3–6. 2018.
- ↑ FÉLIX, L. L. et al., Simple Synthesis of Gold-Decorated Silica Nanoparticles by in Situ Precipitation Method with New Plasmonic Properties, SN Appl. Sci., 3, 443. 2021.
- ↑ BAGHERI, E. et al., Silica Based Hybrid Materials for Drug Delivery and Bioimaging, J. Control. Release, 277, 57. 2018.
- ↑ XU, J. et al., Multifunctional Yolk-Shell Mesoporous Silica Obtained via Selectively Etching the Shell: A Therapeutic 18 Nanoplatform for Cancer Therapy, ACS Appl. Mater. Interfaces, 10, 24440. 2018.
- ↑ CHENG, B. et al., Gold Nanosphere Gated Mesoporous Silica Nanoparticle Responsive to Near-Infrared Light and Redox Potential as a Theranostic Platform for Cancer Therapy, J. Biomed. Nanotechnol, 12, 435. 2016.
- ↑ PARK, J. H. et al., Tunable Aggregation of Gold-Silica Janus Nanoparticles to Enable Contrast-Enhanced Multiwavelength Photoacoustic Imaging in Vivo, Nanoscale, 10, 15365. 2018.
- ↑ YANG, S. et al., Rodlike MSN@Au Nanohybrid-Modified Supermolecular Photosensitizer for NIRF/MSOT/CT/MR Quadmodal Imaging- -Guided Photothermal/Photodynamic Cancer Therapy, ACS Appl. Mater. Interfaces, 11, 6777. 2019.
- ↑ CAI, C. et al., Polydopamine-Coated Gold Core/Hollow Mesoporous Silica Shell Particles as a Nanoplatform for Multimode Imaging and Photothermal Therapy of Tumors, Chem. Eng. J., 362, 842–850. 2019.
- ↑ FÉLIX, L. L. et al., Simple Synthesis of Gold-Decorated Silica Nanoparticles by in Situ Precipitation Method with New Plasmonic Properties, SN Appl. Sci., 3, 443. 2021.
- ↑ BAGHERI, E. et al., Sensors Design Based on Hybrid Gold-Silica Nanostructures, Biosens. Bioelectron, 153, 112054. 2020.
- ↑ NECHIKKATTU, R. & HA, C. S., Tunable Catalytic Activity of Gold Nanoparticle Decorated SBA-15/PDMAEMA Hybrid System, J. Porous Mater, 27, 611. 2020.
- ↑ LI, Y. et al., Implantation of Fe3O4 Nanoparticles in Shells of Au@m-SiO2 Yolk@Shell Nanocatalysts with Both Improved Recyclability and Catalytic Activity, Langmuir, 33, 7486. 2017.
- ↑ NECHIKKATTU, R. & HA, C. S., Temperature-Responsive Mesoporous Silica Nanoreactor with Polymer Gatings Immobilized Surface via a ‘Grafting-to’ Approach as Peroxidase-like Catalyst, Micropor. Mesopor. Mater, 306, 110472. 2020.
- ↑ BYOUN, W. et al., Synthesis and Application of Dendritic Fibrous Nanosilica/Gold Hybrid Nanomaterials, ChemistryOpen, 7, 349. 2018.
- ↑ FEYNMAN, R. P., There’s Plenty of Room at the Bottom, Eng. Sci., XXIII (5). 1960.
- ↑ TANIGUCHI, N., On the Basic Concept of ‘Nano-Technology’, Proc. Intl. Conf. Prod. Eng. Tokyo, Part II, Japan Society of Precision Engineering. 1974.
- ↑ DREXLER, K. E., Engines of Creation : The Coming Era of Nanotechnology, Anchor Books, Doubleday. 1986.
- ↑ https://twitter.com/britishmuseum/status/1110566063245271040?lang=sv.
- ↑ DANIEL, M.-C. & ASTRUC, D., Gold Nanoparticles: Assembly, Supramolecular Chemistry, Quantum-Size-Related Properties, and Applications toward Biology, Catalysis, and Nanotechnology, Chem. Rev., 104, 293. 2004.
- ↑ LOOS, M., Chapter 1 - Nanoscience and Nanotechnology, Carbon Nanotube Reinforced Composites, CNR Polymer Science and Technology, Elsevier, 1–36. 2015.
- ↑ SU, S. & JOKERST, J. V., Chapter 14 - Silica/Gold Hybrid Nanoparticles for Imaging and Therapy, Hybrid Nanomaterials: Design, Synthesis, and Biomedical Applications, CRC Press. 2017.
- ↑ STÖBER, W. et al., Controlled Growth of Monodisperse Silica Spheres in the Micron Size Range, J. Colloid Interface Sci., 26, 62. 1968
- ↑ VALLET-REGÍ, M. et al., Engineering mesoporous silica nanoparticles for drug delivery: where are we after two decades?, Chem. Soc. Rev., 51, 5365. 2022.
- ↑ DANIEL, M.-C. & ASTRUC, D., Gold Nanoparticles: Assembly, Supramolecular Chemistry, Quantum-Size-Related Properties, and Applications toward Biology, Catalysis, and Nanotechnology, Chem. Rev., 104, 293. 2004.
- ↑ SU, S. & JOKERST, J. V., Chapter 14 - Silica/Gold Hybrid Nanoparticles for Imaging and Therapy, Hybrid Nanomaterials: Design, Synthesis, and Biomedical Applications, CRC Press. 2017.
- ↑ SARFRAZ, N. & KHAN, I., Plasmonic Gold Nanoparticles (AuNPs): Properties, Synthesis and their Advanced Energy, Environmental and Biomedical Applications, Chem. Asian J., 16, 720. 2021.
- ↑ Dreaden, E. C.; Alkilany, A. M.; Huang, X.; Murphy, C. J.; El-Sayed, M. A., The golden age: gold nanoparticles for biomedicine, Chem. Soc. Rev., 41, 2740. 2012.
- ↑ Wikimedia Commons.
- ↑ VALLET-REGÍ, M. et al., Engineering mesoporous silica nanoparticles for drug delivery: where are we after two decades?, Chem. Soc. Rev., 51, 5365. 2022.
- ↑ BAGHERI, E. et al., Silica Based Hybrid Materials for Drug Delivery and Bioimaging, J. Control. Release, 277, 57. 2018.
- ↑ XU, J. et al., Multifunctional Yolk-Shell Mesoporous Silica Obtained via Selectively Etching the Shell: A Therapeutic 18 Nanoplatform for Cancer Therapy, ACS Appl. Mater. Interfaces, 10, 24440. 2018.
- ↑ NECHIKKATTU, R. & HA, C. S., Temperature-Responsive Mesoporous Silica Nanoreactor with Polymer Gatings Immobilized Surface via a ‘Grafting-to’ Approach as Peroxidase-like Catalyst, Micropor. Mesopor. Mater, 306, 110472. 2020.
- ↑ VALLET-REGÍ, M. et al., Engineering mesoporous silica nanoparticles for drug delivery: where are we after two decades?, Chem. Soc. Rev., 51, 5365. 2022.
- ↑ BAGHERI, E. et al., Silica Based Hybrid Materials for Drug Delivery and Bioimaging, J. Control. Release, 277, 57. 2018.
- ↑ BAGHERI, E. et al., Sensors Design Based on Hybrid Gold-Silica Nanostructures, Biosens. Bioelectron, 153, 112054. 2020.
- ↑ DANIEL, M.-C. & ASTRUC, D., Gold Nanoparticles: Assembly, Supramolecular Chemistry, Quantum-Size-Related Properties, and Applications toward Biology, Catalysis, and Nanotechnology, Chem. Rev., 104, 293. 2004.
- ↑ SU, S. & JOKERST, J. V., Chapter 14 - Silica/Gold Hybrid Nanoparticles for Imaging and Therapy, Hybrid Nanomaterials: Design, Synthesis, and Biomedical Applications, CRC Press. 2017.
- ↑ VALLET-REGÍ, M. et al., Engineering mesoporous silica nanoparticles for drug delivery: where are we after two decades?, Chem. Soc. Rev., 51, 5365. 2022.
- ↑ SARFRAZ, N. & KHAN, I., Plasmonic Gold Nanoparticles (AuNPs): Properties, Synthesis and their Advanced Energy, Environmental and Biomedical Applications, Chem. Asian J., 16, 720. 2021.
- ↑ Dreaden, E. C.; Alkilany, A. M.; Huang, X.; Murphy, C. J.; El-Sayed, M. A., The golden age: gold nanoparticles for biomedicine, Chem. Soc. Rev., 41, 2740. 2012.
- ↑ MA, D., Chapter 1 - Hybrid Nanoparticles: An Introduction, em Noble Metal-Metal Oxide Hybrid Nanoparticles: Fundamentals and Applications, Noble Metal-Metal Oxide Hybrid Nanoparticles Fundamentals and Applications, Micro and Nano Technologies, Elsevier, 3–6. 2018.
- ↑ CHAUDHURI, R. G. & PARIA, S., Core/Shell Nanoparticles: Classes, Properties, Synthesis Mechanisms, Characterization, and Applications, Chem. Rev., 112, 2373. 2012.
- ↑ CHAUDHURI, R. G. & PARIA, S., Core/Shell Nanoparticles: Classes, Properties, Synthesis Mechanisms, Characterization, and Applications, Chem. Rev., 112, 2373. 2012.
- ↑ MA, D., Chapter 1 - Hybrid Nanoparticles: An Introduction, em Noble Metal-Metal Oxide Hybrid Nanoparticles: Fundamentals and Applications, Noble Metal-Metal Oxide Hybrid Nanoparticles Fundamentals and Applications, Micro and Nano Technologies, Elsevier, 3–6. 2018.
- ↑ DANIEL, M.-C. & ASTRUC, D., Gold Nanoparticles: Assembly, Supramolecular Chemistry, Quantum-Size-Related Properties, and Applications toward Biology, Catalysis, and Nanotechnology, Chem. Rev., 104, 293. 2004.
- ↑ SU, S. & JOKERST, J. V., Chapter 14 - Silica/Gold Hybrid Nanoparticles for Imaging and Therapy, Hybrid Nanomaterials: Design, Synthesis, and Biomedical Applications, CRC Press. 2017.
- ↑ VALLET-REGÍ, M. et al., Engineering mesoporous silica nanoparticles for drug delivery: where are we after two decades?, Chem. Soc. Rev., 51, 5365. 2022.
- ↑ SARFRAZ, N. & KHAN, I., Plasmonic Gold Nanoparticles (AuNPs): Properties, Synthesis and their Advanced Energy, Environmental and Biomedical Applications, Chem. Asian J., 16, 720. 2021.
- ↑ Dreaden, E. C.; Alkilany, A. M.; Huang, X.; Murphy, C. J.; El-Sayed, M. A., The golden age: gold nanoparticles for biomedicine, Chem. Soc. Rev., 41, 2740. 2012.
- ↑ DANIEL, M.-C. & ASTRUC, D., Gold Nanoparticles: Assembly, Supramolecular Chemistry, Quantum-Size-Related Properties, and Applications toward Biology, Catalysis, and Nanotechnology, Chem. Rev., 104, 293. 2004.
- ↑ SARFRAZ, N. & KHAN, I., Plasmonic Gold Nanoparticles (AuNPs): Properties, Synthesis and their Advanced Energy, Environmental and Biomedical Applications, Chem. Asian J., 16, 720. 2021.
- ↑ TURKEVICH, J. et al., A study of the nucleation and growth processes in the synthesis of colloidal gold, Discuss. Faraday Soc., 11, 55. 1951.
- ↑ DANIEL, M.-C. & ASTRUC, D., Gold Nanoparticles: Assembly, Supramolecular Chemistry, Quantum-Size-Related Properties, and Applications toward Biology, Catalysis, and Nanotechnology, Chem. Rev., 104, 293. 2004.
- ↑ SU, S. & JOKERST, J. V., Chapter 14 - Silica/Gold Hybrid Nanoparticles for Imaging and Therapy, Hybrid Nanomaterials: Design, Synthesis, and Biomedical Applications, CRC Press. 2017.
- ↑ VALLET-REGÍ, M. et al., Engineering mesoporous silica nanoparticles for drug delivery: where are we after two decades?, Chem. Soc. Rev., 51, 5365. 2022.
- ↑ SARFRAZ, N. & KHAN, I., Plasmonic Gold Nanoparticles (AuNPs): Properties, Synthesis and their Advanced Energy, Environmental and Biomedical Applications, Chem. Asian J., 16, 720. 2021.
- ↑ Dreaden, E. C.; Alkilany, A. M.; Huang, X.; Murphy, C. J.; El-Sayed, M. A., The golden age: gold nanoparticles for biomedicine, Chem. Soc. Rev., 41, 2740. 2012.
- ↑ STÖBER, W. et al., Controlled Growth of Monodisperse Silica Spheres in the Micron Size Range, J. Colloid Interface Sci., 26, 62. 1968
- ↑ DANIEL, M.-C. & ASTRUC, D., Gold Nanoparticles: Assembly, Supramolecular Chemistry, Quantum-Size-Related Properties, and Applications toward Biology, Catalysis, and Nanotechnology, Chem. Rev., 104, 293. 2004.
- ↑ SU, S. & JOKERST, J. V., Chapter 14 - Silica/Gold Hybrid Nanoparticles for Imaging and Therapy, Hybrid Nanomaterials: Design, Synthesis, and Biomedical Applications, CRC Press. 2017.
- ↑ SARFRAZ, N. & KHAN, I., Plasmonic Gold Nanoparticles (AuNPs): Properties, Synthesis and their Advanced Energy, Environmental and Biomedical Applications, Chem. Asian J., 16, 720. 2021.
- ↑ VALLET-REGÍ, M. et al., Engineering mesoporous silica nanoparticles for drug delivery: where are we after two decades?, Chem. Soc. Rev., 51, 5365. 2022.
- ↑ PARK, J. H. et al., Tunable Aggregation of Gold-Silica Janus Nanoparticles to Enable Contrast-Enhanced Multiwavelength Photoacoustic Imaging in Vivo, Nanoscale, 10, 15365. 2018.
- ↑ PARK, J. H. et al., Tunable Aggregation of Gold-Silica Janus Nanoparticles to Enable Contrast-Enhanced Multiwavelength Photoacoustic Imaging in Vivo, Nanoscale, 10, 15365. 2018.
- ↑ DANIEL, M.-C. & ASTRUC, D., Gold Nanoparticles: Assembly, Supramolecular Chemistry, Quantum-Size-Related Properties, and Applications toward Biology, Catalysis, and Nanotechnology, Chem. Rev., 104, 293. 2004.
- ↑ SARFRAZ, N. & KHAN, I., Plasmonic Gold Nanoparticles (AuNPs): Properties, Synthesis and their Advanced Energy, Environmental and Biomedical Applications, Chem. Asian J., 16, 720. 2021.
- ↑ Dreaden, E. C.; Alkilany, A. M.; Huang, X.; Murphy, C. J.; El-Sayed, M. A., The golden age: gold nanoparticles for biomedicine, Chem. Soc. Rev., 41, 2740. 2012.
- ↑ FÉLIX, L. L. et al., Simple Synthesis of Gold-Decorated Silica Nanoparticles by in Situ Precipitation Method with New Plasmonic Properties, SN Appl. Sci., 3, 443. 2021.
- ↑ BAGHERI, E. et al., Silica Based Hybrid Materials for Drug Delivery and Bioimaging, J. Control. Release, 277, 57. 2018.
- ↑ XU, J. et al., Multifunctional Yolk-Shell Mesoporous Silica Obtained via Selectively Etching the Shell: A Therapeutic 18 Nanoplatform for Cancer Therapy, ACS Appl. Mater. Interfaces, 10, 24440. 2018.
- ↑ CHENG, B. et al., Gold Nanosphere Gated Mesoporous Silica Nanoparticle Responsive to Near-Infrared Light and Redox Potential as a Theranostic Platform for Cancer Therapy, J. Biomed. Nanotechnol, 12, 435. 2016.
- ↑ PARK, J. H. et al., Tunable Aggregation of Gold-Silica Janus Nanoparticles to Enable Contrast-Enhanced Multiwavelength Photoacoustic Imaging in Vivo, Nanoscale, 10, 15365. 2018.
- ↑ YANG, S. et al., Rodlike MSN@Au Nanohybrid-Modified Supermolecular Photosensitizer for NIRF/MSOT/CT/MR Quadmodal Imaging- -Guided Photothermal/Photodynamic Cancer Therapy, ACS Appl. Mater. Interfaces, 11, 6777. 2019.
- ↑ CAI, C. et al., Polydopamine-Coated Gold Core/Hollow Mesoporous Silica Shell Particles as a Nanoplatform for Multimode Imaging and Photothermal Therapy of Tumors, Chem. Eng. J., 362, 842–850. 2019.
- ↑ BAGHERI, E. et al., Sensors Design Based on Hybrid Gold-Silica Nanostructures, Biosens. Bioelectron, 153, 112054. 2020.
- ↑ NECHIKKATTU, R. & HA, C. S., Tunable Catalytic Activity of Gold Nanoparticle Decorated SBA-15/PDMAEMA Hybrid System, J. Porous Mater, 27, 611. 2020.
- ↑ LI, Y. et al., Implantation of Fe3O4 Nanoparticles in Shells of Au@m-SiO2 Yolk@Shell Nanocatalysts with Both Improved Recyclability and Catalytic Activity, Langmuir, 33, 7486. 2017.
- ↑ NECHIKKATTU, R. & HA, C. S., Temperature-Responsive Mesoporous Silica Nanoreactor with Polymer Gatings Immobilized Surface via a ‘Grafting-to’ Approach as Peroxidase-like Catalyst, Micropor. Mesopor. Mater, 306, 110472. 2020.
- ↑ BYOUN, W. et al., Synthesis and Application of Dendritic Fibrous Nanosilica/Gold Hybrid Nanomaterials, ChemistryOpen, 7, 349. 2018.
- ↑ SU, S. & JOKERST, J. V., Chapter 14 - Silica/Gold Hybrid Nanoparticles for Imaging and Therapy, Hybrid Nanomaterials: Design, Synthesis, and Biomedical Applications, CRC Press. 2017.
- ↑ VALLET-REGÍ, M. et al., Engineering mesoporous silica nanoparticles for drug delivery: where are we after two decades?, Chem. Soc. Rev., 51, 5365. 2022.
- ↑ SARFRAZ, N. & KHAN, I., Plasmonic Gold Nanoparticles (AuNPs): Properties, Synthesis and their Advanced Energy, Environmental and Biomedical Applications, Chem. Asian J., 16, 720. 2021.
- ↑ Dreaden, E. C.; Alkilany, A. M.; Huang, X.; Murphy, C. J.; El-Sayed, M. A., The golden age: gold nanoparticles for biomedicine, Chem. Soc. Rev., 41, 2740. 2012.
- ↑ Transforming our World: The 2030 Agenda for Sustainable Development, United Nations. 2015.
- ↑ CUI, R. et al., Engineering Trace AuNPs on Monodispersed Carbonized Organosilica Microspheres Drives Highly Efficient and Low-Cost Solar Water Purification, J. Mater. Chem. A., 8, 13311. 2020.
- ↑ CHENG, B. et al., Gold Nanosphere Gated Mesoporous Silica Nanoparticle Responsive to Near-Infrared Light and Redox Potential as a Theranostic Platform for Cancer Therapy, J. Biomed. Nanotechnol, 12, 435. 2016.
Criada em 20 de Março de 2023
Revista em 27 de Julho de 2023
Aceite pelo editor em 13 de Outubro de 2023

