Carbaniões
Referência : Corrêa, C., (2015) Carbaniões, Rev. Ciência Elem., V3(3):270
Autor: Carlos Corrêa
Editor: José Ferreira Gomes
DOI: [http://doi.org/10.24927/rce2015.270]

[editar] Resumo
Os carbaniões[1], intermediários reativos em muitas reações orgânicas, são aniões em que a carga negativa está associada a um átomo de carbono, embora esteja normalmente deslocalizada sobre outros átomos. São as bases conjugadas de moléculas orgânicas, R-H, por remoção de um protão de uma ligação C-H.
\(R-H+B:\rightarrow R^{\ominus }+BH^{\oplus }\)
No carbanião metilo, \(CH_{3}^{-}\) -, a carga está concentrada no átomo de carbono, mas nos carbaniões cianometilo, \(NC-CH_{2}^{-}\) -, e nitrometilo, \(O_{2}N-CH_{2}^{-}\) -, a carga encontra-se deslocalizada também sobre os grupos ciano e nitro:
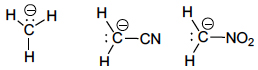
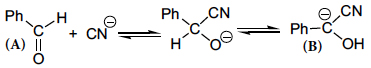
Os carbaniões são normalmente muito reativos, o que lhes confere uma vida bastante curta. A primeira proposta da intervenção de carbaniões como intermediários em Química Orgânica foi apresentada em 1907 por R. W. L. Clarke e A. Lapworth[2] no mecanismo da condensação do benzaldeído (A), catalisada pelo ião cianeto, em que intervém um carbanião (B) intermediário na formação da benzoína, \(Ph-CO-CHOH-Ph\).
Estabilização de carbaniões
A estabilidade dos carbaniões pode ser avaliada pela extensão da reação de remoção de um protão por uma base. O deslocamento deste equilíbrio será tanto maior quanto maior for a estabilidade do carbanião. Assim, para carbaniões mais estabilizados, \(\Delta G^{o}\) é menor, e a reação é mais completa (a constante de acidez, \(K_{a}\), é maior). O carbanião R´–, a que corresponde um menor valor de \(\(\Delta G^{o}\)\) para a remoção de um protão, será mais estabilizado que o carbanião \(R^{-}\).
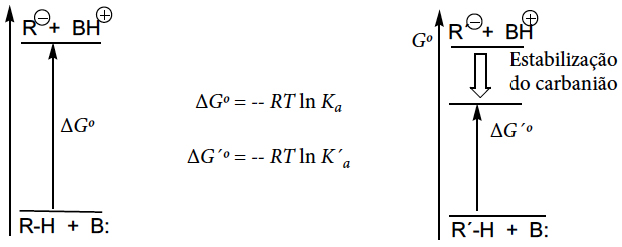
A estabilidade dos carbaniões aumenta se existir um átomo ou grupo de átomos atraidor de electrões ligado ao carbono com carga negativa. Assim, grupos e átomos que exercem efeito indutor –I e mesomérico –M, estabilizam os carbaniões, aumentando a constante de acidez dos ácidos conjugados RH. A TABELA 1 mostra valores da energia de estabilização do carbanião metilo quando se substitui um átomo de hidrogénio.
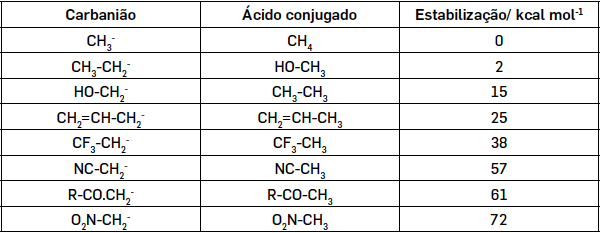
A estabilização dos carbaniões pode, assim, avaliar-se a partir dos valores das constantes de acidez dos respetivos ácidos conjugados. Na literatura estão disponíveis valores de \(pK_{a}\) (\(-log\; K_{a}\)) de muitos ácidos, sendo apresentados alguns na TABELA 2.
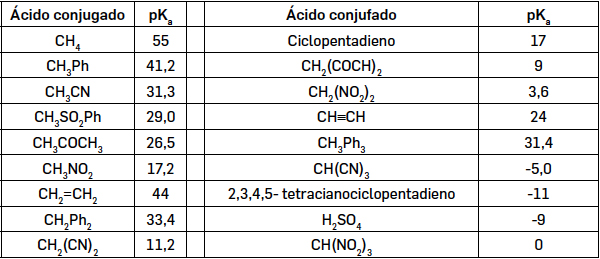
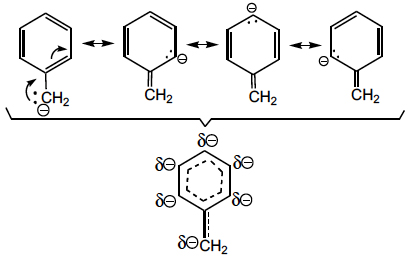
Quanto mais completa for uma reação, menor será o valor de \(pK\). O elevado valor do pKa do metano mostra a dificuldade em se formar o carbanião metilo, em que a carga negativa está praticamente toda localizada no átomo de carbono. À medida que a carga vai sendo deslocalizada (por efeito mesomérico) a estabilidade do carbanião aumente e o valor de \(pK_{a}\) diminui. É o que sucede no carbanião benzilo, onde a deslocalização se estende por todo o anel.
A deslocalização electrónica (mesomerismo, ressonância) e o efeito indutor podem actuar simultaneamente, como sucede com a presença dos grupos ciano, nitro e outros fortemente atraídores de electrões por efeito indutor (– I) e mesomérico (– M) negativos, aumentando a estabilização dos carbaniões, como sucede nos carbaniões cianometilo, fenilsulfonilmetilo, acetilmetilo e nitrometilo. Por esta razão, a sua estabilização é superior à estabilização no carbanião benzilo, em que o efeito indutor é menos significativo. Esta deslocalização electrónica representa-se utilizando as seguintes estruturas contribuintes (ressonância):
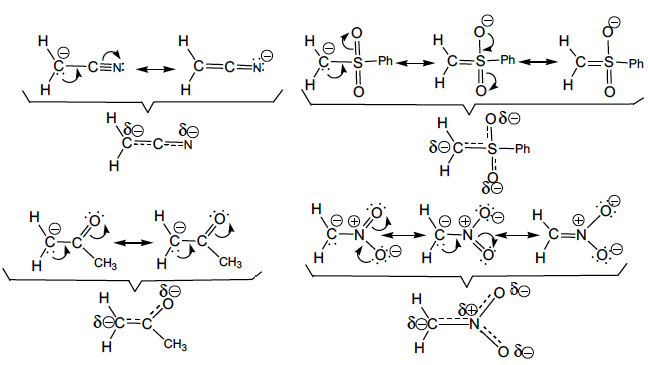
A verdadeira estrutura destes carbaniões é algo parecido com as representações inseridas por baixo das chavetas e significa que na partícula não existem nem ligações duplas, nem ligações simples, nem ligações triplas, mas ligações com carácter intermédio entre duplo e simples e duplo e triplo, que se representaram por traços tracejados sobre traços cheios. Mostra, igualmente, que a carga negativa não está localizada num só átomo mas distribuída pelos átomos de carbono, azoto e oxigénio.
Dos valores das energias de estabilização de carbaniões e dos valores de \(pK_{a}\) apresentados pode deduzir-se a seguinte estabilidade relativa:
\(CH_{3}NO_{2}>CH_{3}COCH_{3}>CH_{3}SO_{2}Ph>CH_{3}CN>CH_{3}Ph\gg CH_{4}\)
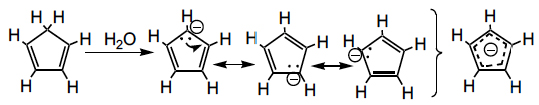
O carbanião derivado do ciclo-hexatrieno é aromático, pois tem \(4n+2\) electrões \(\pi\) deslocalizados num anel, apresentando elevada estabilidade. Se se introduzirem neste carbanião grupos fortemente atraídores de electrões, como quatro grupos ciano, o carbanião passa a ser tão estável que o seu ácido conjugado (\(pK_{a}=-11\)) é mais forte que o ácido sulfúrico (\(pK_{a}=-9\)), dissociando-se completamente na presença de uma base tão fraca como a água.
Geometria de carbaniões
A geometria em torno do átomo de carbono do carbanião metilo é piramidal, como sucede na molécula de amoníaco, devido à presença do par electrónico não ligante do carbono (orbital sp3). As ligações C-H são formadas a partir de orbitais atómicas sp3 do carbono e s do hidrogénio.
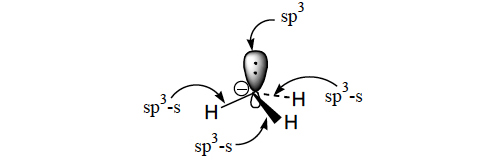
Nos carbaniões benzilo, cianometilo, fenilsulfonilmetilo, acetilmetilo, nitrometilo, alilo e outros a carga negativa está deslocalizada sobre todo o sistema. Para ocorrer esta deslocalização é necessário que o sistema seja plano, como sucede no carbanião alilo, para que os eixos das orbitais atómicas \(p_{z}\) sejam paralelos e possibilitem a formação de orbitais moleculares deslocalizadas, de menor energia.
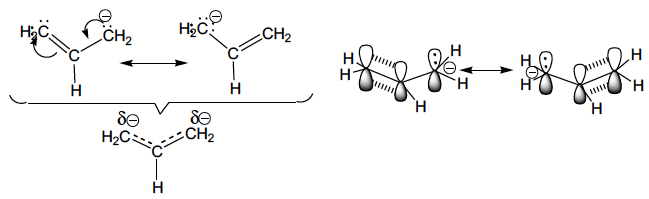
As três orbitais moleculares (OM) \(\pi\) do carbanião resultantes da combinação das três orbitais atómicas p do carbono, são as seguintes:
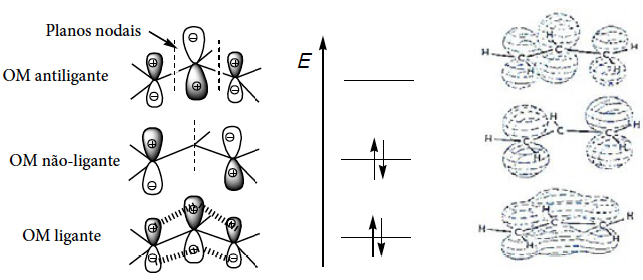
A OM de menor energia está completamente preenchida e estendese sobre todo o sistema, o que confere às ligações C-C um caráter intermédio entre ligação simples e ligação dupla (3 electrões em cada ligação, ou seja, dois electrões \(\sigma \) e um electrão \(\pi\) entre dois carbonos). A OM não-ligante está também completamente preenchida, o que faz com que haja excesso de carga negativa nos átomos de carbono laterais (o que equivale a dizer que é neles onde existe excesso de carga negativa, como as estruturas contribuintes mostram).
Enquanto no carbanião benzilo a carga negativa está deslocalizada sobre o anel, no carbocatião fenilo a carga encontra-se centrada no carbono pois o eixo da orbital sp2 do carbono totalmente preenchida é perpendicular aos eixos das orbitais \(p_{z}\) combinadas no anel, não podendo combinar-se com elas.
Formação de carbaniões
O modo mais comum de formação de carbaniões é a remoção de protões de ligações \(C-H\) por ação de bases. Podem, também, formar-se pela adição de nucleófilos a ligações duplas \(C=C\) desde que existam presentes grupos fortemente atraídores de electrões, como sucede no cianoacrilato de metilo, que polimeriza facilmente na presença de água e vestígios de bases:
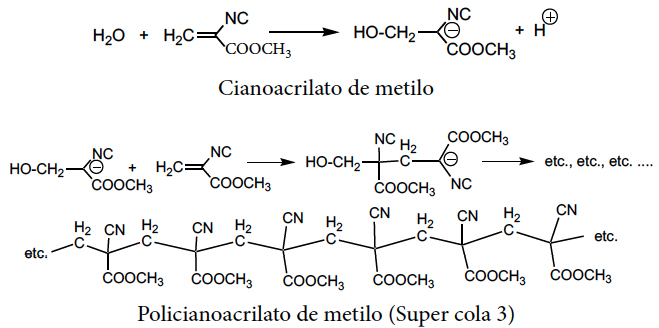
Os compostos organometálicos, como os organomagnesianos, RMgX, e alquillítio, RLi, com ligações metal-C bastante polarizadas, embora não gerem carbaniões livres, reagem do mesmo modo.
Algumas reações em que intervêm carbaniões
- Halogenação de cetonas catalisada por bases.
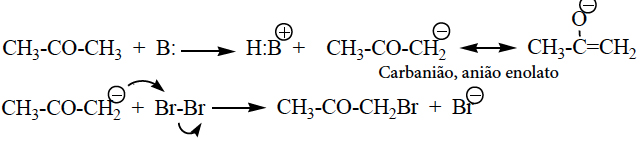
- Condensação alcoólica
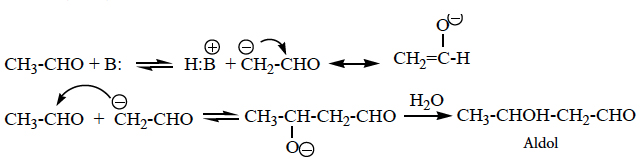
- Condensação de Claisen
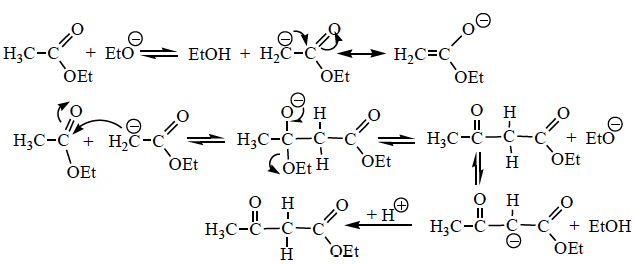
Palavras-chave: Carbanião
[editar] Referências
- ↑ CAREY, F. A. & SUNDBERG, R. J. Advanced Organic Chemistry, Part A, pp 373-390; parte B, pp1-10, 2ª edição, Plenum Press. 1984.
- ↑ CLARKE, W. R. & LAPWORTH A. J.Chem. Soc., Transactions, 91, 694. 1907.
Criada em 15 de Maio de 2015
Revista em 18 de Maio de 2015
Aceite pelo editor em 30 de Setembro de 2015

