ppm e ppb
Referência : Lima, L.S., (2015) ppm e ppb, Rev. Ciência Elem., V3(2):141
Autor: Luis Spencer Lima
Editor: Jorge Gonçalves
DOI: [http://doi.org/10.24927/rce2015.141]

Partes por milhão (ppm) e partes por bilião (ppb) são formas particulares de exprimir fracção mássica e fracção volúmica usadas, em geral, quando estas grandezas adimensionais apresentam valores muito baixos. Partes por milhão (ppm) representa uma parte de soluto por um milhão (106) de partes de solução e partes por bilião (ppb) representa uma parte de soluto por um bilião (1012) de partes de solução. Para designar partes por milhão expressas em volumes costuma utilizar-se o símbolo ppm(V).
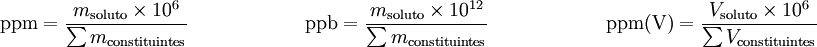
Atendendo a que 1 kg = 1  106 mg, 1 g = 1
106 mg, 1 g = 1 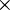 106
106 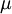 g, será:
g, será:
1 ppm = 1 mg(soluto) por kg(solução) = 1 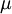 g(soluto) por g(solução)
g(soluto) por g(solução)
Atendendo a que 1 kL = 1 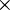 106 mL e 1 L = 1
106 mL e 1 L = 1 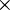 106
106 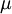 L, e considerando os volumes aditivos, isto é, que o volume da solução é a soma dos volumes dos constituintes, será:
L, e considerando os volumes aditivos, isto é, que o volume da solução é a soma dos volumes dos constituintes, será:
1 ppmV = 1 mL(soluto) por kL(solução) = 1 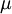 L(soluto) por L(solução)
L(soluto) por L(solução)
Estas formas de exprimir composições de soluções (ou de misturas, em geral) só podem ser utilizadas se as “partes” de soluto e de solução tiverem as mesmas dimensões, isto é, unidades de massa, de quantidade de substância ou de volume. Por exemplo, não é correcto dizer-se que uma solução de naftaleno (soluto) em benzeno (solvente) com uma concentração mássica de 15 mg dm-3 equivale a uma solução com 15 ppm de soluto. Contudo, é frequente a utilização das unidades ppm e ppb em soluções aquosas diluídas para designar a massa de soluto por volume de solução. Tal deve-se ao facto da massa volúmica da solução ser praticamente igual à massa volúmica da água (muito próxima de 1 à temperatura ambiente), o que faz com que 1,0 g de solução ≈ 1,0 g de água ≈ 1,0 cm3. Assim, pode-se considerar que, em soluções aquosas diluídas, 12 mg
dm-3 equivale a uma solução com 15 ppm de soluto. Contudo, é frequente a utilização das unidades ppm e ppb em soluções aquosas diluídas para designar a massa de soluto por volume de solução. Tal deve-se ao facto da massa volúmica da solução ser praticamente igual à massa volúmica da água (muito próxima de 1 à temperatura ambiente), o que faz com que 1,0 g de solução ≈ 1,0 g de água ≈ 1,0 cm3. Assim, pode-se considerar que, em soluções aquosas diluídas, 12 mg dm3 equivalem a 12 ppm.
dm3 equivalem a 12 ppm.
Estas formas de exprimir a concentração são desaconselhadas por parte da União Internacional de Química Pura e Aplicada (IUPAC), devido à ambiguidade existente entre os símbolos, à ambiguidade na propriedade a que se refere a unidade (fracção molar, mássica ou volúmica) e também devido ao facto da designação de ordens de grandezas acima de um milhão poderem ser diferentes entre países. Por exemplo, nos Estados Unidos da América e no Reino Unido, entre outros, 109 denomina-se um bilião, enquanto para a maior parte dos países europeus (entre os quais Portugal) e países da América Latina um bilião significa um milhão de milhões, isto é, 1012. Estas diferenças implicam que 1 ppb em Portugal corresponda a 1000 ppb nos EUA.
Criada em 19 de Maio de 2010
Revista em 14 de Julho de 2010
Aceite pelo editor em 13 de Setembro de 2010
