Diferenças entre edições de "Reagentes e Produtos de reacção"
| Linha 4: | Linha 4: | ||
<span style="font-size:8pt"><b>Editor</b>: <i>[http://www.fc.up.pt/fcup/contactos/ficha_pessoal.php?login=jgoncalv Jorge Gonçalves]</i></span><br> | <span style="font-size:8pt"><b>Editor</b>: <i>[http://www.fc.up.pt/fcup/contactos/ficha_pessoal.php?login=jgoncalv Jorge Gonçalves]</i></span><br> | ||
<span style="font-size:8pt"><b>DOI</b>: <i>[[http://doi.org/10.24927/rce2014.129 http://doi.org/10.24927/rce2014.129]]</i></span><br> | <span style="font-size:8pt"><b>DOI</b>: <i>[[http://doi.org/10.24927/rce2014.129 http://doi.org/10.24927/rce2014.129]]</i></span><br> | ||
| + | <html><a href="https://rce.casadasciencias.org/rceapp/pdf/2014/129/" target="_blank"> | ||
| + | <img src="https://rce.casadasciencias.org/static/images/layout/pdf.png" alt="PDF Download"></a></html> | ||
---- | ---- | ||
<p align='justify'>Um '''reagente''' é uma substância (elemento ou composto) que é consumida no decorrer de uma reacção química. Um '''produto de reacção''' é uma substância formada no decurso de uma reacção química, obtida a partir da combinação dos reagentes.</p> | <p align='justify'>Um '''reagente''' é uma substância (elemento ou composto) que é consumida no decorrer de uma reacção química. Um '''produto de reacção''' é uma substância formada no decurso de uma reacção química, obtida a partir da combinação dos reagentes.</p> | ||
Edição actual desde as 15h50min de 25 de julho de 2019
Referência : Fernandes, R.F., (2014) Reagentes e Produtos de reação, Rev. Ciência Elem., V2(1):129
Autor: Ricardo Ferreira Fernandes
Editor: Jorge Gonçalves
DOI: [http://doi.org/10.24927/rce2014.129]

Um reagente é uma substância (elemento ou composto) que é consumida no decorrer de uma reacção química. Um produto de reacção é uma substância formada no decurso de uma reacção química, obtida a partir da combinação dos reagentes.
Numa reacção os reagentes são as substâncias que se combinam entre si originando novos compostos. Os solventes e os catalisadores, apesar de estarem envolvidos numa reacção não são classificados como reagentes. Considere-se a reacção pela seguinte equação química:
FeS (s) |
+ |
2 HCl (aq) |
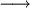 |
FeCl2 (aq) |
+ |
H2S (g) |
O reagente sólido “sulfureto de ferro(II)” combina-se com o reagente “cloreto de hidrogénio” em solução aquosa dando origem aos produtos “cloreto de ferro” em solução aquosa e “sulfureto de hidrogénio” gasoso. Note-se que nesta reacção a água está presente como solvente (“aq”) mas não é referida como reagente.
Alguns reagentes são usados como substâncias de teste (reagentes analíticos) para verificar a presença de compostos específicos. Por exemplo, para se verificar a presença de açúcares redutores usa-se o reagente de Fehlings ou o reagente de Tollens. Em síntese orgânica utilizam-se os reagentes de Grignard, de Felton e de Collins que apresentam funções específicas que promovem uma determinada transformação num substrato orgânico.
O grau de pureza de um reagente descreve a pureza que a substância apresenta para ser utilizada em diferentes aplicações, como por exemplo, em análise química, em síntese ou em testes físicos. O grau de pureza dos reagentes é fixado por organizações internacionais como a ASTM International (originalmente conhecida por American Society for Testing and Materials), a ISO (International Organization for Standardization) ou o NIST (National Institute of Standards and Technology).
Os reagentes com grau de pureza elevado são geralmente empregues em química fina, em laboratórios de análise química e em laboratórios de investigação e desenvolvimento (I&D). No entanto, na química industrial pesada, em que se processam elevadas quantidades (na ordem das toneladas), os reagentes geralmente apresentam graus de pureza menores.
Quando se efectuam reacções químicas, o objectivo é, normalmente, o de obter determinados produtos, com os melhores rendimentos e máxima pureza, sob as melhores condições de segurança e menores danos para o ambiente. Para isso é necessário estudar as reacções, estabelecendo os factores de temperatura, pressão e castálise mais adequados o que é de grande importância na Indústria, em que os aspectos económicos são fundamentais.
A caracterização de todos os produtos, mesmo os que se formam em quantidades reduzidas, é fundamental no estabelecimento dos mecanismos das reacções. Por exemplo, a detecção de pequenas quantidades de dímeros do tipo R-R é indicação da participação de radicais livres R• na reacção em estudo.
Criada em 17 de Fevereiro de 2010
Revista em 12 de Agosto de 2010
Aceite pelo editor em 13 de Setembro de 2010
